



在生物医药的创新浪潮中,抗体药物偶联物(ADC)与以PROTAC为代表的靶向蛋白降解技术(TPD)无疑是近年最受关注的两大技术顶流。ADC实现了化疗药物的“精准投送”,开创了肿瘤靶向治疗的新范式;而PROTAC则从“抑制功能”跃迁至“物理清除”,让攻克“不可成药”靶点成为可能。由此,降解剂-抗体偶联药物(Degrader-Antibody Conjugates, DAC)应运而生,正成为生物偶联药领域最具潜力的下一代创新方向。美迪西正凭借其在ADC和PROTAC领域的双向技术积累,成为DAC药物研发的天然赋能平台。
2026年5月1日,生物医药史迎来历史性一刻——美国FDA正式批准由Arvinas与辉瑞联合开发的VEPPANU(Vepdegestrant),用于治疗ESR1突变的ER+/HER2-晚期乳腺癌。这不仅是PROTAC技术历经二十余年探索后的首次获批,更标志着靶向蛋白降解疗法正式迈入临床应用阶段。至此,PROTAC成为继ADC之后又一个获得临床验证的重大技术范式。
与旨在阻断蛋白质功能的传统小分子抑制剂不同,PROTAC技术利用细胞自身的处理系统——泛素-蛋白酶体系统,将致病蛋白彻底降解。
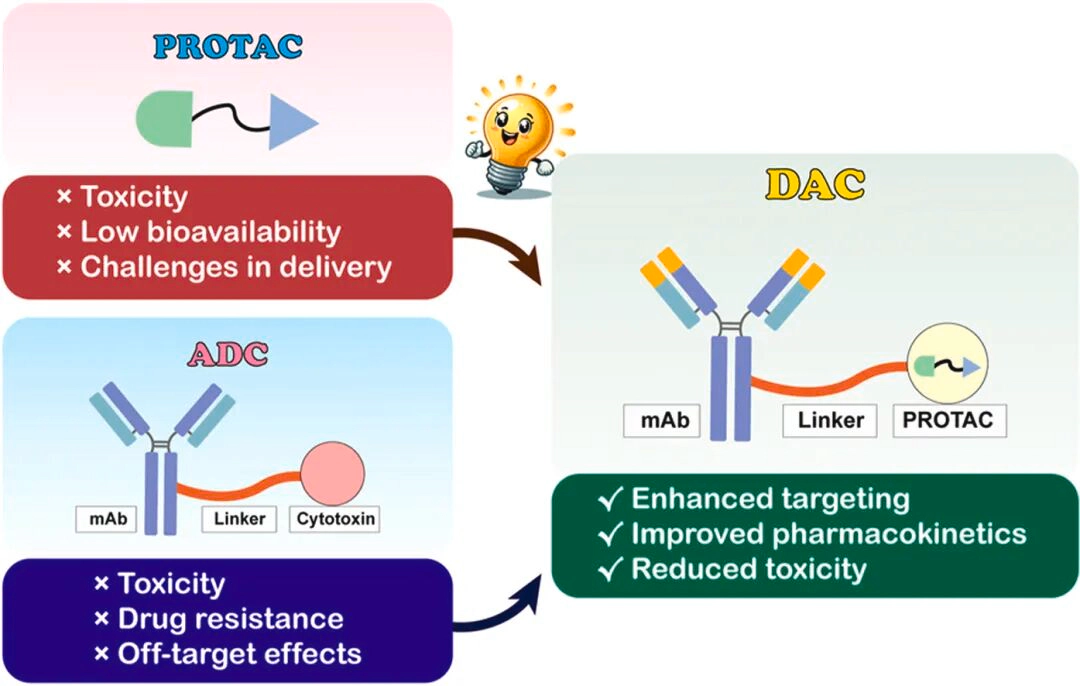
然而,PROTAC作为独立药物仍面临显著短板:分子量大导致口服生物利用度低,正常细胞与癌细胞无差别暴露带来脱靶毒性,以及“钩状效应”影响降解效率等问题,限制了其应用潜力。DAC正是为解决这些问题而生。
DAC由单克隆抗体与蛋白降解剂(如PROTAC或分子胶)通过化学连接子偶联而成。其作用机制如下:抗体负责精准识别肿瘤细胞表面抗原,DAC-细胞复合物被内吞后,连接子在细胞内被酶切释放活性降解剂;降解剂充当桥梁,将致病蛋白与E3泛素连接酶强行结合,通过泛素-蛋白酶体系统实现靶蛋白的彻底降解。
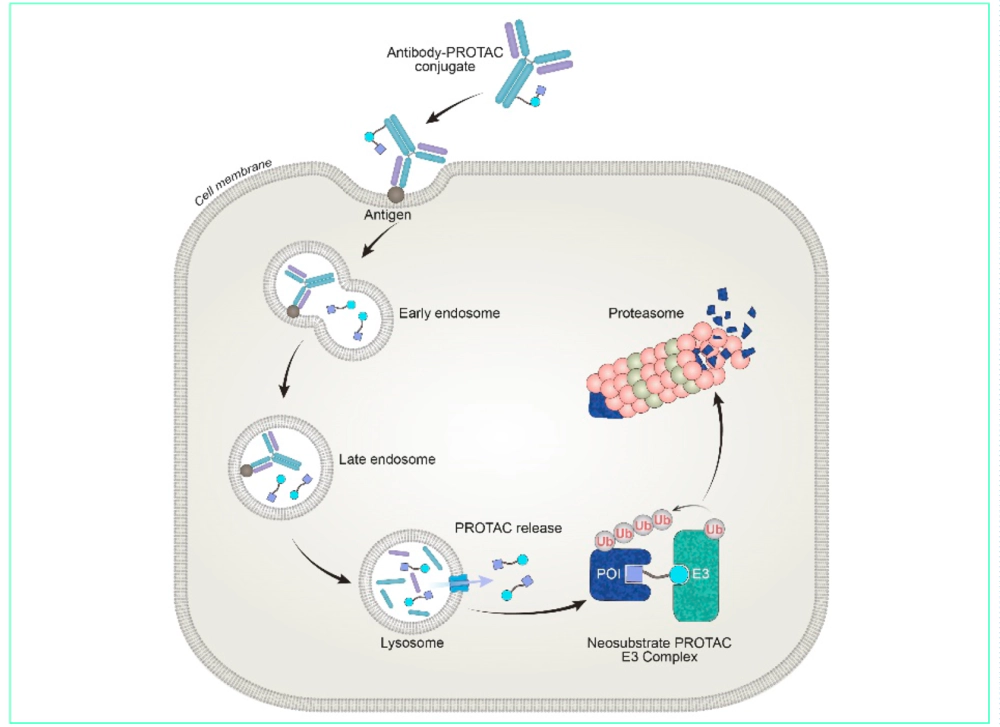
Mechanism of DAC[1]
相较于ADC,DAC的核心优势主要体现在三个层面——
作用机制突破:从阻断功能迈向物理清除,有望克服传统小分子药物及ADC常见的耐药问题。
靶点范围扩容:可靶向传统“不可成药”靶点(如支架蛋白、转录因子),且不依赖靶点自身酶活。
递送精准性提升:抗体介导的靶向递送显著降低降解剂的系统暴露与脱靶毒性,同时改善口服PROTAC生物利用度低的问题。
目前,可构建DAC的降解剂类型有PROTAC(利用泛素-蛋白酶体系统)、LYTAC(溶酶体靶向嵌合体,适用于膜蛋白)和AUTAC(自噬靶向嵌合体)等,为DAC在肿瘤、自免、神经退行性疾病等领域的应用拓展了广阔空间。
当前DAC领域正处于快速升温阶段——
2026年4月9日,罗氏与美国生物制药公司C4 Therapeutics宣布达成战略合作,共同开发DAC疗法,交易总金额超过10亿美元。这一重大交易标志着DAC正式进入跨国药企的战略视野。
2026年4月美国癌症研究协会(AACR)年会上,Orum Therapeutics公布了新一代DAC候选药物ORM-1153的临床前数据。该药物靶向CD123,携载GSPT1降解剂,在低剂量下即展现出强效抗白血病活性,且在一系列急性髓系白血病(AML)患者样本和TP53突变模型中保持了降解活性,支持其向临床开发阶段推进。
在中国,DAC的布局同样加速。2026年初,杭州和正医药与美国一家生物技术公司达成DAC药物全球合作伙伴关系,实现了中国Biotech在DAC领域的首笔海外授权交易,标志着本土DAC开始走向全球舞台。
DAC融合了抗体工程、小分子合成、生物偶联与蛋白降解四大核心技术,其开发复杂度远超传统药物。这意味着,具备一站式、多平台整合能力的CRO合作伙伴将成为DAC研发的关键赋能者。
作为深耕生物医药临床前研发二十余年的CRO领军企业,美迪西已前瞻性地搭建了覆盖ADC、PROTAC、抗体、寡合苷酸、CGT、多肽等新分子药物的特色研发服务平台,助力651件IND获批临床,其中包含33个ADC药物和7个PROTAC药物。美迪西正凭借其在ADC和PROTAC领域的双重技术积累,成为DAC药物研发的天然赋能平台。
在ADC领域,美迪西提供从Payloads合成、药物偶联到药效学、药代动力学及安全性评价的一站式临床前服务,可涵盖抗体、连接子和毒素的选择及偶联策略优化、体外功能评估与体内药效验证。截至目前,已成功助力33个ADC药物获批临床。
美迪西与宜联生物的深度合作堪称典范。美迪西深度参与了宜联生物TMALIN技术平台的建设,完成了有效载荷C24、C57及连接子-有效载荷B81的首次合成,并开发了从价廉易得原料出发的高效合成工艺路线。该平台已成为宜联生物B7H3 ADC授权罗氏5.7亿美元首付款合作的核心基石。这一案例不仅展现了美迪西在ADC研发中的深厚积累,更为DAC药物的开发奠定了坚实的偶联技术基础。
推荐阅读:助力创新药物出海+1!美迪西祝贺宜联生物B7H3 ADC授权罗氏 | Bilingual
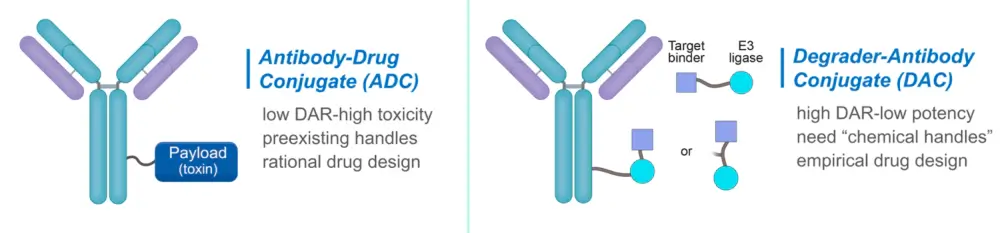
Description of ADC and DAC[1]
在PROTAC领域,美迪西同样建立了从Idea到IND的全方位研发服务平台。核心服务涵盖PROTAC分子设计与合成(分析E3连接酶表达与功能、优化连接子长度与化学性质、支持高通量筛选)、靶向蛋白降解全面验证(体外降解实验、竞争实验确认机制、功能研究评估细胞功能影响、组学分析揭示全局调控)以及体内药理药效、药代动力学及安全性评价等。
截至目前,美迪西已助力7个PROTAC药物进入临床阶段,其中包括为信诺维的全球首创口服蛋白降解剂XNW34017提供了符合GLP标准的体内外药代与安评试验服务。
推荐阅读:全球首创、靶向AURKA、降解MYC!美迪西助力合作伙伴信诺维口服蛋白降解剂XNW34017获批临床
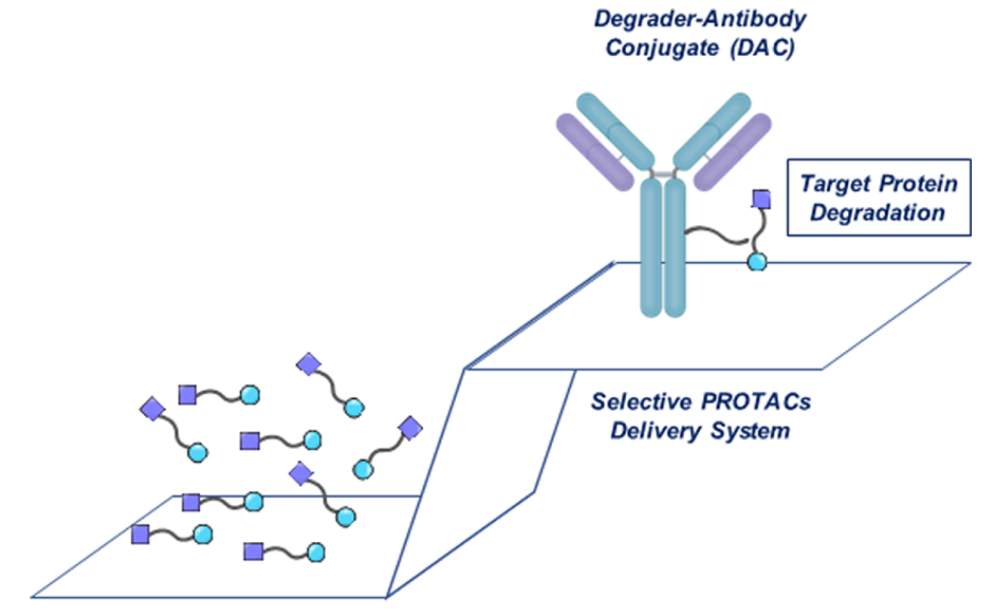
PROTACs Delivery System[1]
随着VEPPANU成功上市验证PROTAC成药路径、罗氏等行业巨头重金押注DAC,以及具备ADC和PROTAC双向技术积淀的一站式CRO平台加速赋能,DAC药物正在从科学构想加速驶入临床开发的快车道。未来几年将是DAC技术从概念验证走向临床验证的关键窗口期。
DAC不仅是ADC与PROTAC的简单相加,更是一种全新的治疗逻辑:用抗体的精准,赋予降解剂以方向;用降解剂的机制,突破传统药物的边界。伴随着MNC的强劲布局与以美迪西为代表的CRO平台的持续赋能,DAC将为攻克肿瘤耐药、拓展治疗边界提供全新利器。
参考文献:
[1] Ki Bum Hong, Hongchan An. Degrader-Antibody Conjugates: Emerging New Modality. Review J Med Chem. 2023 Jan 12;66(1):140-148. doi: 10.1021/acs.jmedchem.2c01791.
[2] Yaolin Guo, et al. What influences the activity of Degrader-Antibody conjugates (DACs). Eur J Med Chem. 2024 Mar 15:268:116216. doi: 10.1016/j.ejmech.2024.116216.
[3] Yam B Poudel, et al. The New Frontier: Merging Molecular Glue Degrader and Antibody-Drug Conjugate Modalities To Overcome Strategic Challenges. J Med Chem. 2024 Sep 26;67(18):15996-16001. doi: 10.1021/acs.jmedchem.4c01289.
 相关新闻
相关新闻