




近年来,欧盟EMA对"替代传统动物模式 (Replacement)、减少动物使用 (Reduction)、优化实验设计(Refinement)"(3Rs) 的推动不遗余力。美国FDA更是积极鼓励人工智能 (AI)、体外人源类器官等新替代方法(NAMs)的研发与应用,将其作为提升药物非临床评估效率、降低研发成本、契合伦理要求的重要方向。在此背景下,NAMs如何在药物非临床评估中实际应用?面临哪些技术挑战?又将为产业带来怎样的改变?
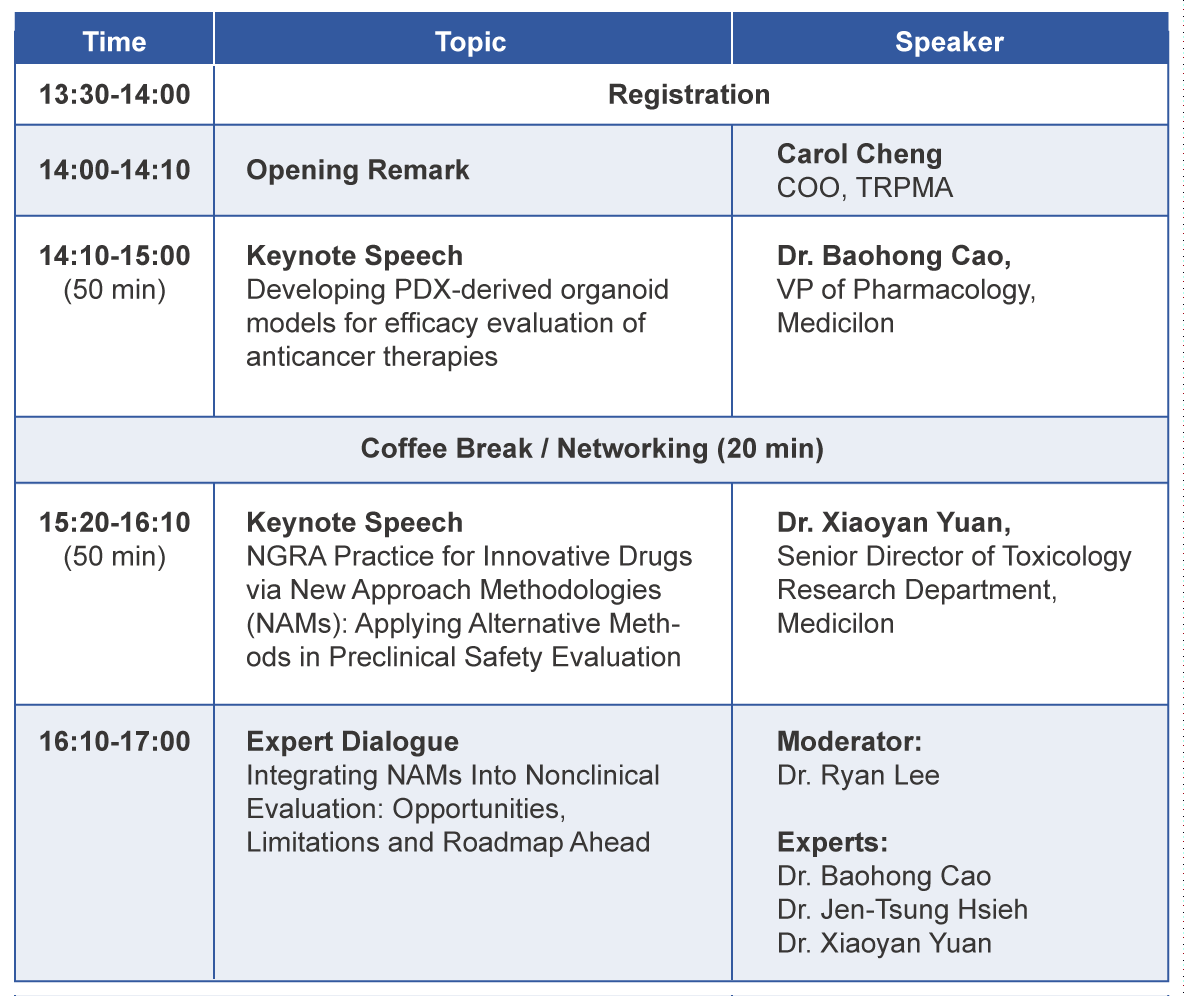
为回答这些关键问题,帮助生物医药专业人员了解产业最新进展,Medicilon与TRPMA合作,将于12月12日下午共同举办「Applications and Challenges of NAMs in Nonclinical Drug Evaluation」新药研发论坛。特别邀请美迪西药理部副总裁曹保红博士、毒理学副总裁谢仁宗博士、毒理研究部高级主任苑晓燕博士、及台湾商务拓展副总监李一麟博士,从技术框架、适用场景、实战案例到未来趋势,为业者提供系统化、可实施的研究方案。
NAMs简介:技术体系与监管趋势。深入解析NAMs技术框架,涵盖体外、化学模拟、计算机模拟等方法,结合监管机构的法规要求,对比分析用于药物毒性研究的NAMs模型。
应用的药物类别:精准定位适用范围。针对双特异性抗体、CAR-T 细胞治疗产品、小分子药物、抗病毒药物等类别,精准分类,阐明不同药物类别研发策略的科学依据。
实践案例:从策略选择到结果分析。通过代表性案例详细解读NAMs在新药临床前研究中的实施路径,包括策略制定与结果评估等关键环节,提供可参考的技术参考与实务指引。
挑战与展望:现实难点与未来趋势。客观剖析目前NAMs应用中面临的技术瓶颈、法规差异、资料认可度等挑战;展望NAMs在技术、人才发展和法规体系完善等方面的发展趋势,助力企业提前布局。
本次论坛全程免费,诚邀业界同仁及专家学者莅临参与,汇聚智慧,共探非临床研究的创新路径!
主办单位 | 美迪西、台湾研发型生技新药发展协会 (TRPMA)
地点 | TRPMA会议厅 (台北市南港区忠孝东路六段465-1号1楼)
时间 | 2025年12月12日(星期五)14:00-17:00
报名方式:点击文末「报名链接」跳转报名(免费)
联络人:叶映君 Vian Yeh (02)2783-1262 trpma@trpma.org.tw
曹保红 博士 药理部副总裁
北京医科大学医学博士。曾在丹麦国家血清研究所、美国匹兹堡大学及匹兹堡儿童医院、美国贝纳罗亚研究所等从事研究工作,在 NATURE CELL BIOLOGY, NATURE BIOTECHNOLOGY, JOURNAL OF CELL BIOLOGY等国际顶级学术期刊发表论文多达24篇,所研究项目曾两次获得获美国国立卫生研究院重要课题(NIH R01)资助。加入美迪西之前,曹博士曾担任药明康德美国分公司免疫肿瘤学高级主任,MI BIORESEARCH(现由科文斯收购)研究运营总监,上海睿智化学研究有限公司、诺华(中国)生物医学研究中心等的高级管理职务。超25年医药研发经验,超10年团队管理经验,曹博士在药物发现领域造诣深厚,尤其在肿瘤疾病模型构建和CAR-T细胞治疗方面颇有建树。
谢仁宗 博士 DABT 毒理学副总裁
美国密西西比大学医学中心药理和毒理学博士,美国毒理学委员会认证毒理学家,曾任台湾国科会、科技部和经济部的药品开发计划审查委员、台北医学大学及台湾生技产业深耕学院讲师。谢博士扎根医药行业30余载,其中12年在台湾CDE的工作经验。谢博士曾负责审评IND和NDA申请案之药理和毒理试验报告,撰写审评报告及进行风险评估,审评的IND案件超过200件,其中生物制剂药品约70件;NDA案件超过150件,其中生物制剂药品约40件,还曾草拟台湾CDE非临床安全性试验指导原则、ICH S9和E14 / S7B以及多个台湾非临床安全性试验指导原则。此外,谢博士在药理毒理研究、疾病动物模型的建立、新药全流程研发等方面也颇有经验。这些经验将进一步推动美迪西毒理研究的发展,提高项目申报的质量、效率和成功率。加入美迪西之前,谢博士曾在江西龙昌药业有限公司、龙行生物药业(杭州)有限公司、合一生技股份有限公司等担任高管,磨砺出卓越的新药研发经验和团队管理经验。
苑晓燕 博士,研究员 毒理研究部高级主任
从业十五年,深耕药物等产品非临床安全性评价与法规毒理学,聚焦细胞基因治疗产品,助力近 10 个产品通过 IND 申报;主持国家级课题 4 项,以第一 / 通讯作者发表 SCI 论文 11 篇,参编专著 3 部。获中国毒理学家资格及美国 DABT 资质,兼任中国毒理学会理事等学术职务。
李一麟 博士 台湾商务拓展副总监
毕业于英国诺丁汉大学,获得药学博士学位。他在监管事务方面有 20 年的奉献精神,曾连续三年为一家脂质体公司实现“每年一个 IND”的公司目标,并获得生物仿制药的 MAA 批准,目前他正在台湾大学攻读精英 MBA,目标是弥补行业采用“只开发不研究”模式的差距。
 相关新闻
相关新闻会议时间:2023年10月19-20日
会议地点:广州花都皇冠假日酒店