



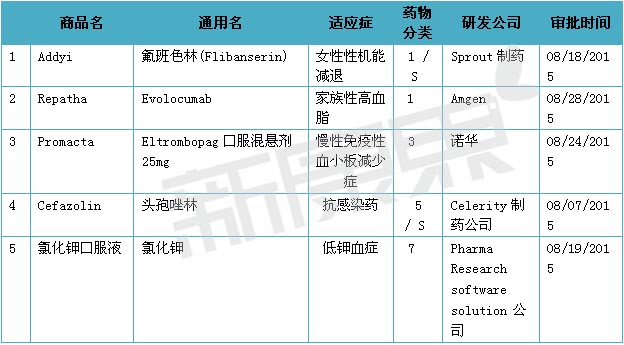
2015年08月份美国FDA共审批通过5种新药,1类新分子实体药物2个; 3类新剂型药物1个; 5类新规格或新生厂商药物1个;7类已上市但未经NDA批准的药品1个。
一、女性性机能减退新分子实体药物Addyi(氟班色林)
2015年08月18日,美国FDA批准了Sprout制药公司的女性性机能减退新分子实体药物Addyi(氟班色林)上市。Addyi为口服片,,每片含氟班色林100mg,推荐的使用剂量为每日100mg。特别需要注意的是由于女性服用Addyi后会出现低血压、晕厥、意外受伤、中枢神经系统紊乱的不良反应,因此建议患者在就寝时间服用Addyi。同时由于Addyi与酒精相互作用会增加患者低血压和晕厥的风险,因此患者在服用Addyi时禁止饮酒。
二、降血脂新药Repatha (Evolocumab)
2015年08月28日,美国FDA批准了Amgen公司的降血脂新单克隆抗体药物Repatha (Evolocumab)上市。Repatha为PCSK9抑制剂,PCSK9为前蛋白转化酶枯草溶菌素9蛋白,该蛋白可降低肝脏从血液中清除低密度脂蛋白胆固醇(LDL-C)的能力,而LDL-C被公认为心血管疾病的主要风险因子。Repatha用于原发性高血压患者和纯合子家族性高胆固醇血症。在2015年07月24日,美国FDA批准了赛诺菲安万特的降血脂新单克隆抗体药物Praluent(alirocumab)上市,Praluent同样为PCSK9抑制剂类降脂药。
Repatha为皮下注射剂,规格为140 mg/mL,可在腹部、大腿及上臂区域皮下注射。
美国FDA审批新药主要是根据药物化学类型和治疗潜能来进行分类的。新药按化学类型主要分为:1类新分子实体化合物(NME),创新性最强。指在美国从未作为药品批准或销售的活性成分,可以是单一成分,也可以是立体异构混合物中的一部分;2类新的衍生物。从已上市的活性成分(即所谓“专利”药)化学衍生而来,即已在美国上市的活性成分的酯、盐或其它非共价键衍生物,或者是去修饰基团的母体化合物未在美国批准上市的;3类新剂型。含有已上市活性成分的新剂型或新处方,其适应症可以与上市产品相同,也可以不同;4类新组合物。含有两种或两种以上已上市的活性成分的品种,上市产品中尚无这种组合;5类药物新规格或新生产商;6类新适应症。由同一家公司或其他公司在美国批准或上市的具有新用途的复制品;7类已上市但未经NDA批准的药品。适应症已与上市产品相同,也可不同;8类变为非处方药;10类适应症不同的新的新药申请。
 相关新闻
相关新闻