



本周,科学界共同见证了一场免疫学领域的重大胜利——2025年诺贝尔生理学或医学奖的颁布,恰逢10月12日“世界关节炎日”的到来。这一时间上的巧妙契合,不仅是对基础科学探索者的崇高礼赞,也是对全球数亿关节炎患者的深切关怀。它清晰地揭示了一条从“认识疾病”到“征服疾病”的科学路径:诺贝尔奖所表彰的“外周免疫耐受”机制,正是理解关节炎等自身免疫性疾病根源的钥匙。
通过完善的动物模型库与专业的临床前评价体系,美迪西正助力全球研究人员将诺贝尔级的免疫学洞见,在多种动物模型中进行验证与转化。在这个基础突破与技术实践紧密交汇的时代,我们正共同加速,将关于免疫系统的深刻认知,转化为能够改变全球患者命运的创新疗法。
2025年诺奖:一项变革性的发现

诺贝尔委员会授予Mary E. Brunkow、Fred Ramsdell和Shimon Sakaguchi2025年诺贝尔奖,以表彰他们在外周免疫耐受方面的开创性工作。他们的共同研究揭示了人体免疫系统如何被阻止攻击自身组织——这对于理解和治疗包括关节炎在内的自身免疫性疾病而言是一项至关重要的发现。Shimon Sakaguchi教授特别指出,他对调节性 T 细胞 (Treg) 的研究“与我们如何预防类风湿性关节炎等疾病的发展息息相关”。
Treg对于建立和维持免疫自身耐受至关重要。它们的基因异常或功能变异是各种单基因和多基因自身免疫性疾病的病因。基于Treg重建自身耐受有望在临床上治愈自身免疫性疾病。如何建立和维持对自身抗原的免疫无反应状态(即免疫自身耐受)以防止病理性自身免疫,以及如何重建自身耐受来治疗自身免疫性疾病是免疫学中最基本的问题之一。
Treg最初是在啮齿动物中发现的,它们是天然存在的、抑制性表达CD25的CD4+ T细胞,积极参与维持外周自身耐受:从正常免疫系统中特异性去除 CD25+CD4+ T 细胞会导致与人类类似的多种自身免疫性疾病的自发发展,而这些疾病可以通过重建相同的细胞群成功预防(见图A)。
后来发现这些CD25+CD4+ Tregs特异性表达转录因子FoxP3,作为Treg功能的主控制器。 Foxp3+CD25+CD4+ Tregs已被确立为一个功能和表型均独特的T细胞亚群。过去数十年的研究已清晰地表明Foxp3+ Tregs在控制多种病理和生理性免疫反应中至关重要。大多数Treg由正常胸腺生理性产生,形成功能成熟且独特的T细胞亚群(胸腺衍生型Treg),并持续存在于外周,功能稳定(见图B)。
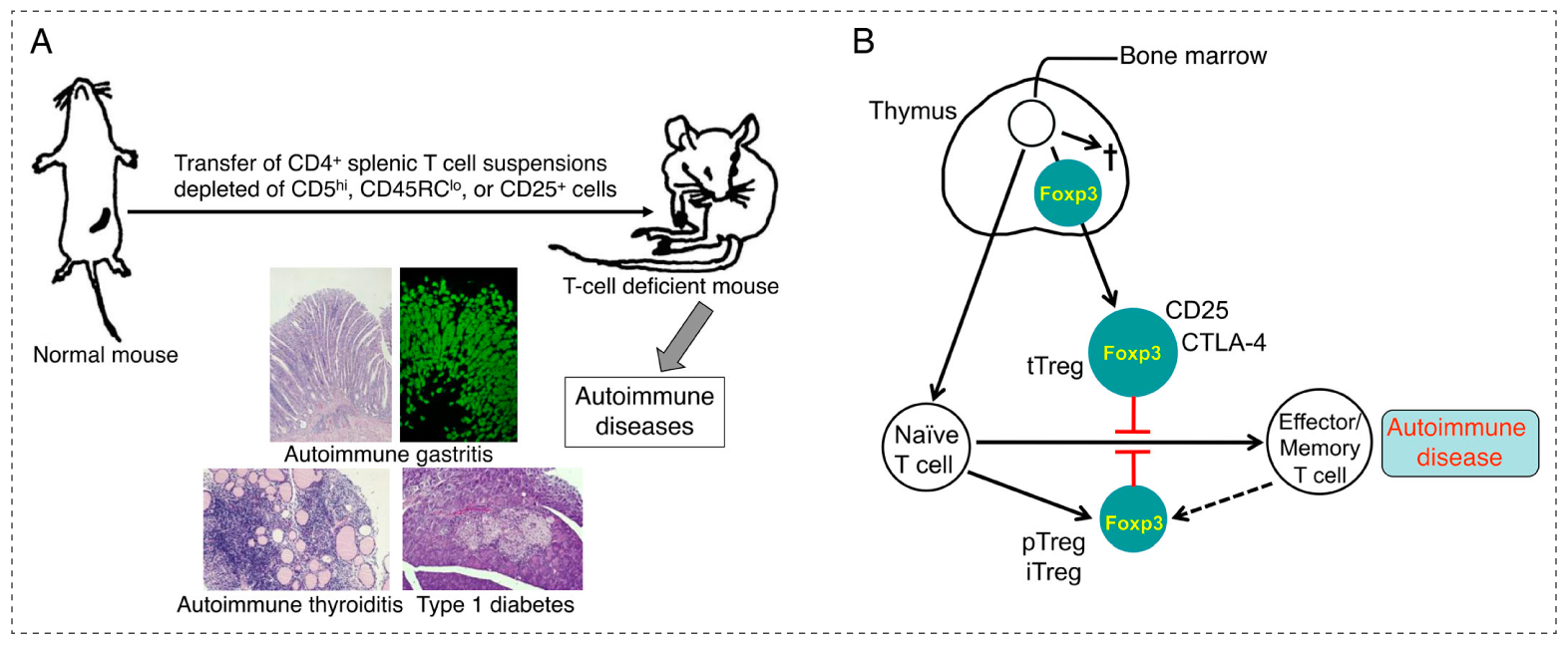
Tregs in immunological self-tolerance and autoimmunity[1]
关节炎的关联:免疫耐受失效
关节炎(Arthritis),尤其是类风湿性关节炎(Rheumatoid Arthritis, RA),是外周免疫耐受机制失效的一个典型例子。诺贝尔奖得主的研究有助于解释为什么免疫细胞会错误地攻击关节组织,从而导致炎症、疼痛和进行性损伤。类风湿性关节炎关节腔内充斥着如TNF-α、IL-6、IL-1等强大的促炎因子。这些细胞因子会直接抑制Treg细胞的抑制功能。例如,TNF-α可以干扰Treg细胞表面TNFR2信号。Treg的功能稳定性依赖于其特异的DNA低甲基化状态。在类风湿性关节炎的慢性炎症环境中,这种稳定的表观遗传特征可能被破坏,导致Treg功能不稳定甚至转变为促炎性的Th17样细胞。在类风湿性关节炎中,滑膜内的抗原呈递细胞(如树突状细胞、巨噬细胞等)被持续激活,高表达CD80和CD86等共刺激分子。与此同时,效应T细胞大量表达其受体CD28。它们共同驱动了免疫反应的持续和炎症的放大,对关节组织造成进行性损伤。
美迪西关节炎研发服务:将发现转化为治疗
美迪西很荣幸能够为这一重要领域做出贡献,提供强大的临床前关节炎模型,帮助研究人员开发新的疗法。美迪西药效部紧跟行业发展与市场需求,不断完善创新,经多年经验累积,多方验证和长期实践考验,建立了完善的动物模型库,在免疫炎症性疾病研究中,可根据客户需求提供和定制各种有效的动物模型,检测药物的有效性。拥有深厚专业理论知识和多年实验经验的专业团队,能利用多种体外和体内研究模型为各类免疫炎症性疾病提供疗效评估。
类风湿性关节炎动物模型是深入研究疾病发病机制与评价药物疗效的关键工具。以下为美迪西在该领域内的部分研究案例分享:
胶原诱导的关节炎模型
胶原诱导的关节炎(Collagen Induced Arthritis, CIA)与人类类风湿关节炎具有共同的免疫学和病理学特征,因此被广泛应用于致病机理和新药药效的研究。Ⅱ型胶原蛋白能够免疫诱导易感啮齿动物和非人灵长类动物体内产生关节炎性质的自身免疫反应。
此外,CIA的易感性也与RA相似,和主要组织相容性复合体(MHC)的Ⅱ类分子有关。免疫反应的特点是:刺激胶原特异性T细胞,产生针对性免疫抗原(异源CⅡ)和自身抗原(小鼠或大鼠CⅡ)的高滴度特异性抗体。
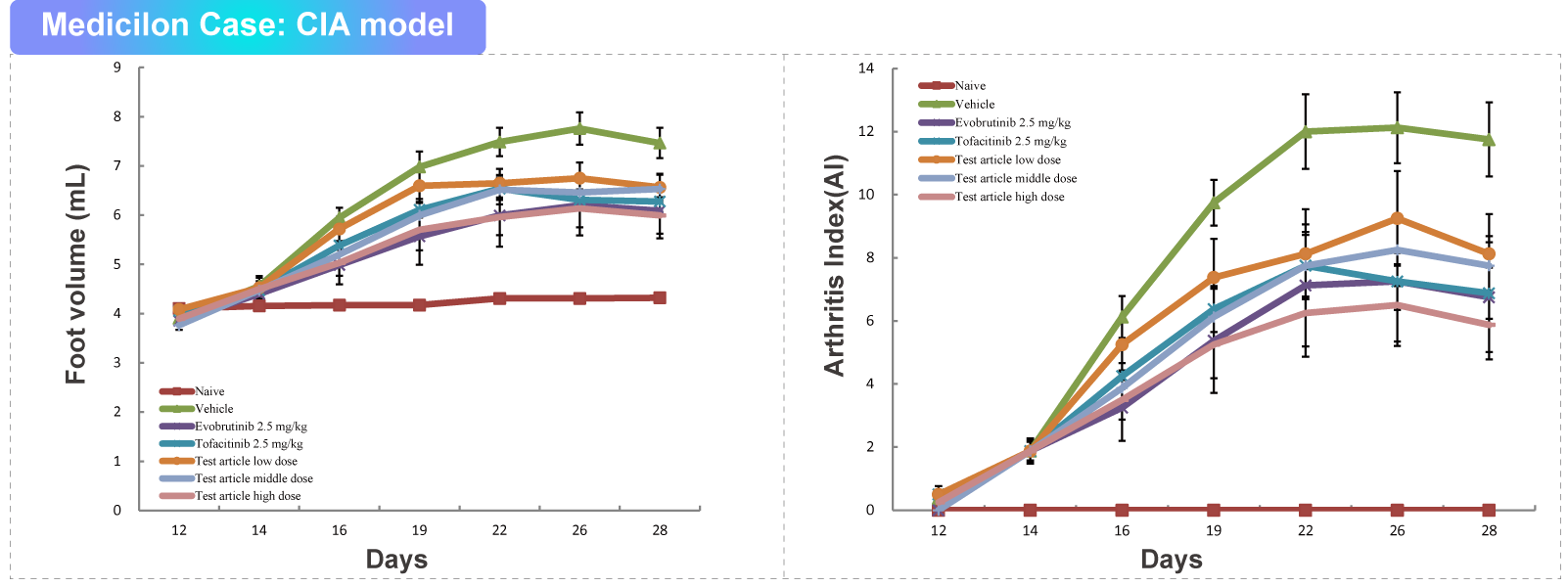
完全弗氏佐剂诱导的关节炎模型
完全弗氏佐剂(Complete Freund’s Adjuvant, CFA)诱导的关节炎模型能够表现出伴有全身性改变的持续性炎症,以及滑膜增生、角膜翼、耳部和尾部出现“关节炎”结节等,与人类关节炎有多种相似之处,因此是一个非常适合用于发病机理的研究和新药药效评价的模型。
CFA是由石蜡油和二缩甘露醇一油酸与热灭活结核分枝杆菌混合而成的混合乳液,在啮齿类动物的爪部皮下注射或腹腔注射,从而诱导动物多器官的免疫炎症反应。CFA诱导的大鼠关节炎应用广泛,对研究炎症过程的病理、生理和药理作用,以及评估药物的镇痛潜力或抗炎作用具有重要意义。
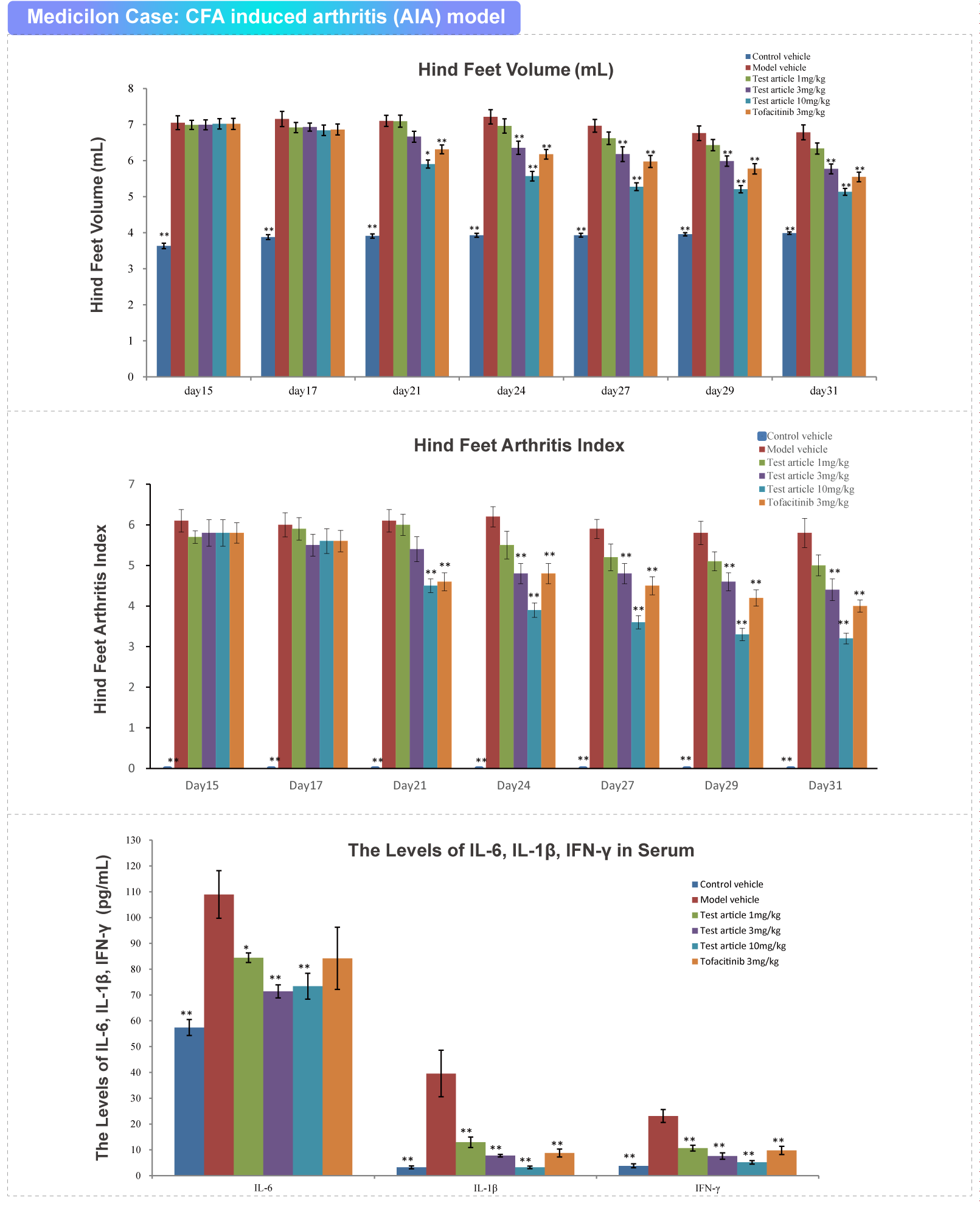
尿酸钠诱导的痛风性关节炎模型
痛风性关节炎(Gouty Arthritis, GA)的主要特征是:尿酸钠晶体在关节周围组织沉积,刺激关节,引起关节滑膜及周围组织病损及炎症反应。临床中,痛风的发病伴随着关节周围组织或关节的触痛、红斑、发红、肿胀、疼痛和发热。
目前,GA发作与缓解的具体机制尚未明确,但研究人员普遍认为,关节部位析出的尿酸钠晶体是造成痛风性关节炎的关键化学物质。尿酸钠晶体能够诱发自身免疫及炎症反应,国际上常被用于诱导急性痛风性关节炎模型,已被广泛应用于药理、药效等方面的研究。
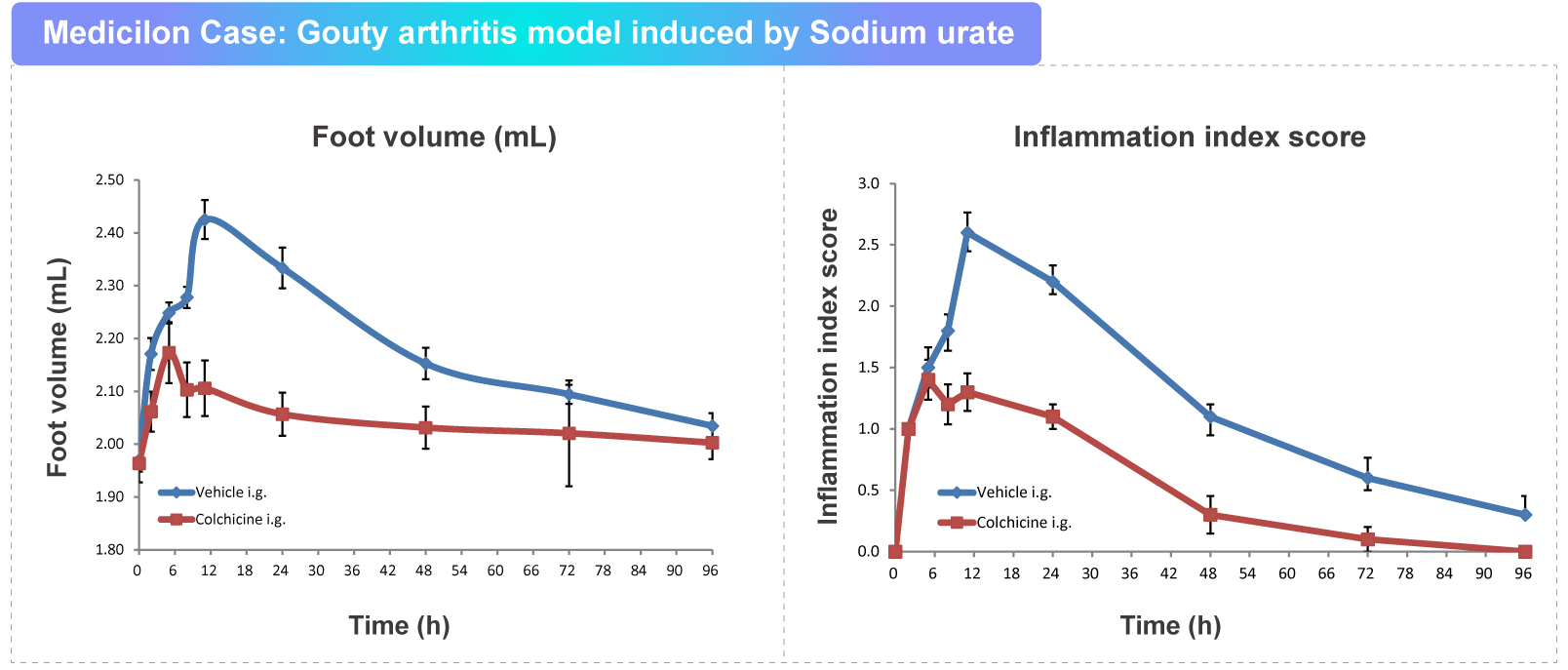
值此世界关节炎日,我们得以清晰地预见:免疫学领域的基础发现——正如今年斩获诺贝尔奖的突破性研究——正在为关节炎治疗开辟全新的可能性。在美迪西,我们能够通过提供可靠的、临床相关的动物模型来支持这一进程,这些模型有助于加速转化为能够真正改变全球患者命运的革新性疗法。
美迪西药理药效部
美迪西药理药效部凭借多年积累的丰富经验,经过多方验证与长期实践,已成功构建包含790+种动物模型的专业化模型库,其中包括510+种肿瘤药效模型及280+种非肿瘤疾病的评估模型(涵盖炎症免疫系统、神经精神系统、消化系统、内分泌及代谢系统、心脑血管系统等疾病领域),能够根据客户的个性化需求,提供多种高效可靠的动物模型。现有实验动物资源丰富,涵盖非人灵长类、犬、大小鼠、兔、豚鼠、小型猪等多个种类。参考文献:[1] Shimon Sakaguchi. Taking regulatory T cells into medicine. J Exp Med. 2021 Jun 7;218(6):e20210831. doi: 10.1084/jem.20210831.
 相关新闻
相关新闻