



前言导读
一年一度的诺贝尔奖再次将全球目光聚焦于科学前沿!今天,2025年诺贝尔生理学或医学奖正式揭晓。Mary E. Brunkow、Fred Ramsdell和Shimon Sakaguchi三位科学家因在外周免疫耐受领域的突破性发现,共同获得2025年诺贝尔生理学或医学奖!
尽管GLP-1研究未能在此次折桂,但科学界普遍认为,这并非因其重要性不足。多位科学家在GLP-1领域的革命性工作,早已具备诺奖级的分量。从发现到转化,这段跨越百年的探索历程,本身已是一部“无冕之王”的传奇。
他们的研究,回答了人类面对肥胖与糖尿病两大全球流行病最迫切的诉求。GLP-1药物不仅能高效安全地降糖、减重,更被证实具有心血管保护等多重益处,惠及全球数亿患者——这恰恰完美契合了诺贝尔遗嘱中“为人类带来最大福祉”的宗旨
从1906年“肠促胰岛素”效应的初现端倪,到1980年代Joel Habener、Svetlana Mojsov等人鉴定出GLP-1的活性形式,再到Lotte Bjerre Knudsen在诺和诺德成功研发出长效药物司美格鲁肽……这条百年探索之路,是基础科学向临床应用转化的完美典范。
20世纪70年代,重组DNA技术的发展为基因发现提供了新工具。Mojsov教授在洛克菲勒大学攻读研究生期间,开发了固相肽合成新方法,使其能够合成短肽激素胰高血糖素。而Habener教授团队利用鮟鱇鱼胰岛细胞文库,成功分离出编码胰高血糖素原的cDNA。序列分析显示,除了胰高血糖素,该cDNA还包含与肠促胰岛素GIP相似的序列。同期,芝加哥大学的Graeme Bell博士也从多种哺乳动物中鉴定出胰高血糖素原cDNA及其基因,证实其包含两个GLP区域:GLP-1和GLP-2,其中GLP-1在哺乳动物中高度保守。
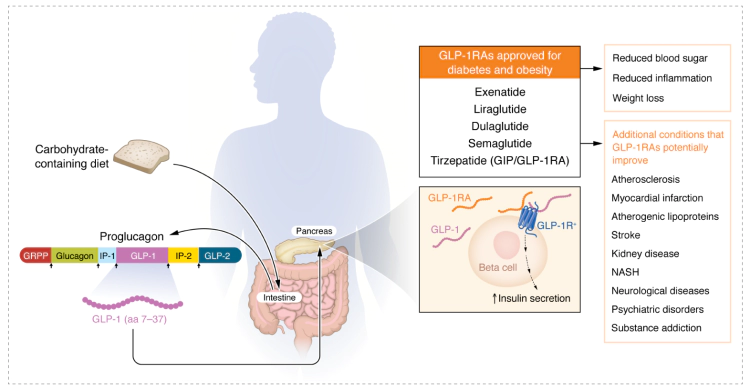
GLP-1 的产生机制及其有益作用[1]
GLP-1是继GIP之后于1983年发现的第二种肠促胰岛素,由胰高血糖素原基因编码,主要由肠道L细胞产生。其在人体内主要以GLP-1(7-36)活性形式存在。GLP-1通过与GLP-1受体(GLP-1R)特异性结合,刺激胰岛素分泌、抑制胰高血糖素释放、延缓胃排空并抑制食欲,在糖尿病治疗中发挥多重积极作用。
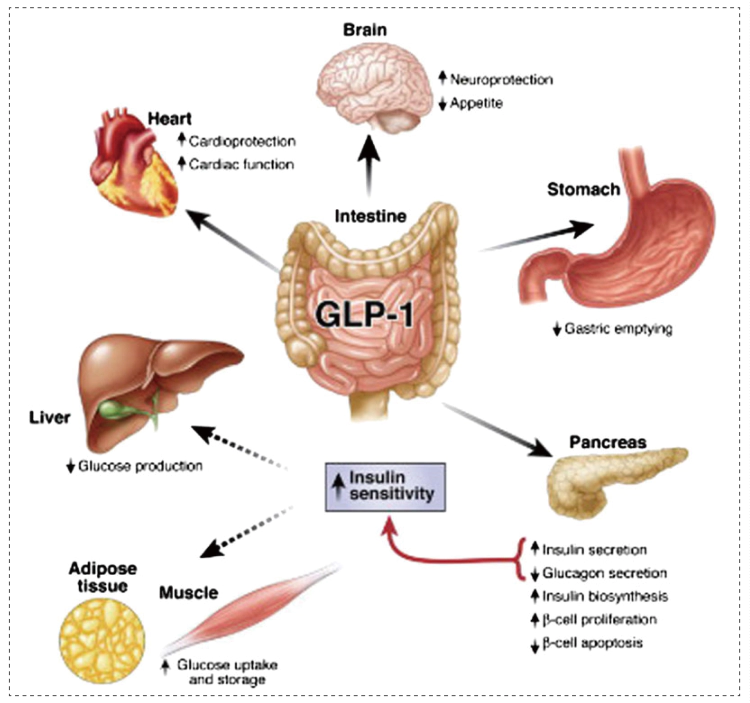
GLP-1的多重生理功能[2]
GLP-1R是2型糖尿病的关键治疗靶点。GLP-1R是一种多效性偶联受体,通过与多种G蛋白偶联来调控细胞通路,最终促进血糖依赖性的胰岛素分泌。这一机制的阐明为后续药物研发奠定了坚实基础。
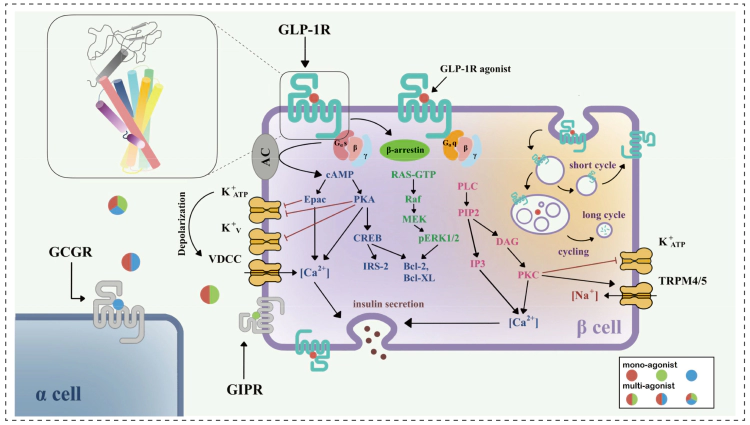
GLP-1R在胰腺β细胞中的信号通路[3]
1984年,Daniel Drucker博士加入Habener教授实验室,开展了一系列关键研究,旨在表征预测的胰高血糖素原产物及其生物活性。他的研究表明,GLP-1的生物活性形式在特定位点被截短,并且在转染的细胞中得到有效加工。随后,Drucker博士在自己的实验室继续深入探索,证明GLP-2是一种肠道生长因子,其类似物替度鲁肽最终于2012年获FDA批准,用于治疗短肠综合征。
与此同时,丹麦的Jens Holst团队正在研究肠道细胞产生的信号分子。他们开发了免疫测定法,证实胰高血糖素原在肠道中被裂解产生两种GLP,并发现截短形式的GLP-1能够刺激胰岛素分泌。后续研究进一步揭示,GLP-1还能抑制胃动力、外分泌功能以及食欲,这些发现为GLP-1激动剂在肥胖治疗中的应用奠定了基础。
当Habener团队专注于分子生物学研究时,Mojsov教授凭借其化学背景采用合成肽的方法来鉴定GLP-1的活性形式。她推测并合成了GLP-1的特定片段,并制备了相应抗体。随后,Mojsov与Drucker、Habener展开合作,利用其抗体在大鼠肠道中鉴定出GLP-1(7-37),并关键性地证明了该肽段能够刺激大鼠胰岛细胞释放胰岛素。这项突破性研究于1987年发表在《Journal of Clinical Investigation》上。
1992年,GLP-1首次进入人体研究,证实其输注可诱导胰岛素分泌,对糖尿病患者和非糖尿病患者均产生抗糖尿病作用。次年,Nauck等人进一步证明,GLP-1输注可使2型糖尿病患者的血糖恢复正常。尽管GLP-1展现出显著疗效,但其半衰期过短限制了临床应用。首个获批的GLP-1RA艾塞那肽源于蜥蜴毒液中的exendin-4,其对DPP-4具有抗性,于2005年获批,最初需每日注射两次,后续开发出每周一次的长效剂型。
为克服半衰期限制,Knudsen教授领导诺和诺德团队致力于开发更稳定的GLP-1RA。她利用白蛋白可逆结合策略,合成了GLP-1的脂肪酸衍生物,成功保护GLP-1免受降解。这一努力催生了利拉鲁肽,首个适合每日一次给药的GLP-1类似物,于2009/2010年相继获EMA和FDA批准。
此后,Knudsen团队继续优化,经过数千次测试,最终研发出司美格鲁肽。该药物与白蛋白结合能力显著增强,半衰期延长约两千倍,可实现每周一次皮下注射。2017年,司美格鲁肽获FDA批准用于糖尿病治疗。令人惊喜的是,当剂量提升至2.4毫克时,其在非糖尿病肥胖人群中实现了平均15%的体重减轻,促使FDA于2021年批准其高剂量版本用于减肥适应症。
今夜,斯德哥尔摩的聚光灯虽未照亮他们,但GLP-1药物在无数患者身上创造的生命奇迹,已是这座殿堂外最闪亮的星光!
诺奖表彰的是科学发现的 “从0到1”,而将伟大构想转化为普惠药物的 “从1到100”,则需要全球生物医药产业的协同努力。在这条GLP-1的长征路上,美迪西深感荣幸能成为前沿科学的赋能者与同行者,更致力于成为诺奖级思想的实践伙伴!
基于GLP-1的科学突破,当前降糖策略已从单纯"控制血糖"转向"改善心血管功能"与血糖控制并重。GLP-1RA因其多重生理作用,已成为糖尿病药物研发的热点领域。
美迪西凭借丰富的实战经验和技术积累,为客户提供GLP-1药物的一站式研发服务方案,涵盖药物发现、药学研究、药效学评价、药代动力学研究及安全性评价等。截至2025年6月底,美迪西已成功助力19个GLP-1药物获批临床,其中多个项目获得中国NMPA、美国FDA及澳洲TGA等多国监管机构批准,另外有多个GLP-1项目在研。
 相关新闻
相关新闻