



美迪西提供整合性的化学、生产与质量控制(CMC)服务,支持药物研发从临床前研究到IND申报、临床试验直至早期商业化的全过程。通过整合原料药(API)工艺开发、制剂开发、分析与质量体系以及GMP生产能力,我们构建了一站式CMC平台,旨在降低监管风险、加快研发进程,并保持长期开发的灵活性。
 CMC开发与研究
CMC开发与研究 专业化
专业化 注册申报支持
注册申报支持GLP设施面积>30万平方英尺
IND成功案例 50+
准时交付 98%
服务客户总数 2000+

专业技能
我们经验丰富的科学家团队在CMC流程的每个阶段均具备丰富的专业经验:
凭借在专业能力与基础设施方面的持续投入,美迪西的CMC(化学、生产与质量控制)部门全面赋能药物开发过程的各个阶段,以实现更高的效率与合规性。
先进的设施平台
我们配备大规模综合设施,满足现代制药研发的高标准需求:

我们通过对原料药(API)、制剂开发与生产制造的统一整合,消除各开发阶段之间的衔接障碍。
一站式CMC服务
集原料药、制剂、分析方法、稳定性研究和GMP生产于一体的综合平台。
阶段适配策略
提供定制化CMC策略,贯穿临床前研究、I/II期临床试验直至商业化阶段,并随项目进展动态优化。
无缝衔接
构建一体化CRO到CDMO的工作流程,打破信息孤岛,降低技术转移风险。
质量源于设计(QbD)
以QbD理念为核心,开展稳健的工艺与制剂开发,确保产品质量与法规合规性。
卓越的法规支持能力
在支持IND、NDA及DMF申报方面拥有成熟经验,服务全球监管机构。
先进的基础设施
配备符合GMP规范的先进设施,集成先进分析技术与生产制造能力。
从CRO向CDMO的转移过程中,往往会导致数据丢失和进度延误。我们的集成化服务模式可确保从首克样品到最终商业化批次,完整保留分子开发的知识与数据积累。
了解更多服务内容,欢迎联系我们
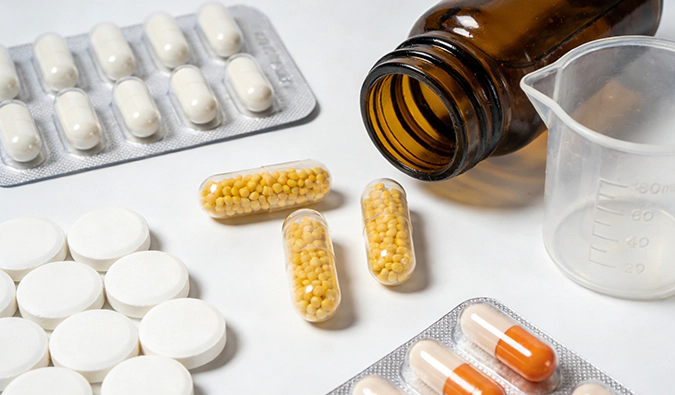
美迪西原料药工艺部门为创新药和仿制药项目提供覆盖全流程的原料药CMC服务,涵盖从合成路线设计与实验室合成到工艺放大及GMP生产的各个环节,并符合全球监管要求。

从合成路线筛选到工艺验证,我们的科研团队致力于开发稳健且可放大的化学工艺。
实现向GMP生产的无缝工艺转移,并提供全生命周期的验证支持,确保工艺在放大生产中的稳定性与一致性。
起始物料开发
定制开发关键起始物料,从源头保障供应链稳定性与质量可控性。
合成路线设计与筛选
进行全面的合成路线筛选和确认,实现最佳收率与纯度。
工艺优化
基于试验设计(DoE)进行工艺优化,实现从克级到公斤级的高效放大。
杂质谱研究
开展杂质及遗传毒性杂质的结构解析,并建立科学的控制策略。
我们支持临床前及临床阶段的API开发,采用符合GMP规范的工艺,满足IND支持性研究及早期临床用药供应需求。

实验室确认
开展实验室工艺确认及关键工艺参数界定。
非GMP中试
进行非GMP条件下的中试批生产,用于获取早期放大数据。
毒理批次
生产用于毒理学研究的专用批次。
cGMP生产
开展符合cGMP要求的原料药生产,用于临床试验。
法规文件
提供用于中国(NMPA)及美国(FDA)申报的CMC相关资料与文件。
法规合规支持
为中国(NMPA)和美国(FDA)申报提供专家支持,并提供完整的CTD格式文件。
选择稳健且可放大的合成路线对原料药质量和商业化成功至关重要。美迪西以质量源于设计(QbD)理念为核心,确保您的产品顺利研发。
我们的策略不仅局限于合成开发,而是从五大关键维度进行系统评估,为不同开发阶段量身定制稳定且具备商业可行性的工艺路线。
技术可行性
对反应动力学、安全性特征及关键工艺参数进行严格评估,确保结果的可重复性。
供应链保障
评估原材料来源的稳定性、成本效益及长期供应连续性,以支撑持续生产。
可放大性
确保实验室规模工艺可无缝转移至中试及商业化生产设备,且不影响收率。
绿色化学
通过减少废弃物与溶剂使用,满足全球可持续发展标准,降低环境影响。
知识产权策略
开展全面的自由实施(FTO)分析,保障知识产权安全,规避侵权风险。
与我们讨论您的项目
通过严格的盐筛选、多晶型鉴定及结晶工艺开发,提升药物性能。从实验室到上市全程支持。

研发核心平台
我们的的集成化平台支持平行筛选与并行开发,缩短进入临床阶段的时间。
我们提供全套支持专利申报的技术成果及稳定性研究,确保您的分子为下一阶段开发做好充分准备。
美迪西结合化学合成与酶催化工艺,实现高效的原料药(API)生产——专为复杂分子设计。
工艺开发
基于特定合成路线,提供端到端的酶催化工艺开发。
筛选与优化
开展高通量生物酶筛选及反应条件优化,以实现最大产率。
丰富的酶库
可即时获取多样化酶类资源,用于快速测试:酮还原酶、亚胺还原酶、硝基还原酶、酯酶、酰胺酶、转氨酶、脂肪酶
分析方法
建立并验证稳健的分析方法,以确保工艺受控与产品纯度。
GMP放大
实现向符合 GMP 要求的生产设施的无缝技术转移,用于生物催化放大生产。
生物催化为现代原料药(API)合成提供战略性优势,在遵循绿色化学原则的同时,实现更优的工艺表现。
了解更多服务内容,欢迎联系我们
美迪西制剂部门提供端到端的制剂 CMC 服务,覆盖口服制剂、注射剂及特殊剂型的各个开发阶段。

剂型
口服固体制剂、注射剂、半固体制剂、液体制剂及特殊剂型。
起始物料开发
定制化起始物料开发,从源头保障供应链稳定性与质量一致性。
工艺优化
基于试验设计(DoE)的工艺优化与放大,实现从克级到千克级的高效转化。
合成路线设计与筛选
系统开展合成路线筛选与验证,以实现最佳收率与纯度。
杂质谱分析
针对基因毒性杂质及相关杂质,开展先进的结构解析与控制策略开发。
面向复杂递送需求的高端制剂技术。
针对难溶性药物的解决方案:
实现缓释及改良释放行为:
靶向及复杂给药途径
Medicilon 拥有符合 GMP 标准的 API 及口服固体制剂生产设施,可实现从研发到临床生产的无缝衔接。
配备先进的分析实验室与完善的质量体系,确保数据完整性与可靠性。
提供符合 FDA、NMPA 及全球监管要求的可申报 CMC 文件。

案例 1:12 个月完成 IND 申报(小分子 NCE)
美迪西为一项小分子新化学实体(NCE)项目提供了全流程、一体化的 CMC 服务,通过基于质量源于设计(QbD)的阶段适配策略,并与 FDA 和 NMPA 的监管要求保持一致,自合同签署起约 12 个月内完成 IND 申报并获批。通过优化合成路线、实施 GMP 生产以及准备可用于申报的 CMC 文件,该项目支持了中美 IND 的高效并行申报,同时最大程度降低了注册风险。
案例 2:合成路线、固态形态与杂质控制优化(小分子 API)
Medicilon针对一项小分子原料药(API)项目,对其合成路线、固态策略及杂质控制体系进行了系统性重构。通过一体化 CMC 方法,显著提升了工艺的可制造性、安全性及分析方法的稳健性。通过简化合成路线、优化固态晶型选择,以及强化杂质与溶剂控制,该项目实现了显著的收率提升,并建立了可放大、受控良好的 API 生产工艺,为后续开发奠定了坚实基础。
专业的注册支持助力简化您的申报流程
美迪西(Medicilon)的注册事务专家可优化复杂的审批路径,确保符合全球监管要求。
我们的专业能力
美迪西不仅是临床前研发服务提供商,更是您值得信赖的创新合作伙伴。凭借20余年的行业经验,我们整合先进技术、科学专长和卓越的注册合规能力,加速药物开发进程并提升成功率,助力您的愿景落地实现。
立即联系我们,与我们一起迈出下一步,预约咨询
CMC 规划应尽早在先导化合物优化阶段启动,以降低后续开发风险,并避免在 IND 申报前发生不必要的返工。
美迪西提供一站式的原料药和制剂CMC(化学、制造和控制)服务,所有环节均在同一质量体系下进行,从而提升协同效率并减少交接过程中的错误。
Medicilon 提供符合 CTD 标准的 CMC 文件,支持向 FDA、NMPA 及其他全球监管机构提交申报资料,包括CTD 模块 3的准备工作。
即根据项目所处开发阶段匹配相应的开发深度——既满足当前监管要求,又避免在后续阶段之前产生不必要的成本投入。
一体化模式可减少技术转移过程中的断层,提升数据与工艺知识的连续性,并缩短从研发到 GMP 生产的整体周期。
美迪西提供 DMF 编制服务以及符合 CTD 格式的申报资料,支持中美双报需求,并涵盖稳定性研究与方法验证支持。