创新是一个民族进步的灵魂,是一个国家兴旺发达的不竭动力。在化学药物领域,我国《药品注册管理办法》界定的1类新药则代表了国家创新药物的研制水平,是挑战最大的化药创新。面对着1类新药漫长的研发与申报周期,巨大的研发成本与不可预知的研发风险,能让制药企业一掷千金地专注于1类新药研发的最大动力,莫过于药品上市后带来的巨大商业回报。
9月8日-10日,药智网携手中国药房杂志社联合主办的《2017中国医药创新高峰论坛•暨医药企业研发实力百强榜单发布》在重庆耀世启幕,会议将隆重发布《2017年药品研发实力排行榜》(包括其子榜《2017中国化药研发实力排行榜》),哪些是医药行业的领军企业?哪些将凭借夯实的化药研发实力入围“化药榜”?欢迎大家莅临会场观摩。
本文参考 “药智药品注册与受理数据库”、相关的新闻报道,搜集了近20年内获得CFDA批准的国产1类化学药品信息,对其市场表现进行了分类点评,借以了解1类新药上市后对制药企业带来的商业回报。
一、不负所望篇
1、埃克替尼
埃克替尼是由浙江贝达药业有限公司研发,并于2011年6月初获CFDA批准的我国首个具有自主知识产权的小分子靶向抗癌药(药用其盐酸盐片剂,商品名:凯美纳),被前卫生部部长陈竺评价为“民生领域堪比两弹一星的重大突破”。埃克替尼的第一个适应证是晚期非小细胞肺癌(NSCLC)。凯美纳的第一个适应症是晚期非小细胞肺癌(NSCLC),肺癌是全世界范围内各种恶性肿瘤中的第一杀手,也是自2005年以来中国位居第一的死亡病因,而NSCLC约占所有肺癌患者的85%。一项头对头Ⅲ期临床试验结果证实,埃克替尼对NSCLC的治疗效果与吉非替尼,但其价格却远低于国内占主导地位的NSCLC治疗药物-吉非替尼与厄洛替尼。
根据药智网提供的2017年7月26日重庆市药品招标信息,0.125g规格埃克替尼片单价为61.62元/片,而同期中标的厄洛替尼片(进口)与吉非替尼片(国产)单价分别为474.28元/片与158.5元,而进口吉非替尼片于2017年7月初在江西的中标价为235.8元/片。
2014年,埃克替尼治疗EGFR突破的适应证获批准,2017年埃克替尼与实现国产化的吉非替尼、达沙替尼、伊马替尼进入国家医保目录。
市场独占情况
贝达药业针对埃克替尼进行了全面的专利布局,以其化合物专利(专利号:03108814.7,下文简称814’号专利)为核心,但该专利却屡遭国内自然人或企业的专利挑战。
2014年9月,付某针对814’号专利向专利复审委员会提出无效宣告请求,认为该专利的权利要求1-14的技术方案在说明书中未公开,不符合专利法第二十六条第三款的规定。随后在2014年11月,自然人王某也向专利复审委员会提出无效宣告请求,认为该专利的权利要求1-14的修改不符合专利法第三十三条的规定;权利要求1-14的技术方案不符合专利法第二十六条第三款的规定;权利要求1-7、10-14得不到说明书的支持,不符合专利法第二十六条第四款的规定;权利要求1-14不符合专利法第二十二条第三款的规定。其实早在2011年9月,就曾有公司针对该专利提出过专利权无效宣告请求,但在口头审理结束后双方便达成和解,该公司撤销了无效宣告请求。
2015年10月9日,专利复审委员会做出第27258号决定,表示维持814’号专利继续有效。
目前,埃克替尼及其片剂国内仅有贝达药业一家生产。
市场表现
《知识产权报》于2016年7月报道上述专利无效案时援引数据称,埃克替尼先后于2013年、2014年、2015年为贝达药业带来了4.75亿元、7.03亿元与9.13亿元的收入。另有多个专业媒体均报道称,埃克替尼2016年销售额已超过10亿元。
2、丁苯酞
丁苯酞是由中国医学科学院药物研究所和石家庄制药集团有限公司等单位共同研发的我国第一个拥有自主知识产权的脑血管疾病治疗药物,于2004年11月正式投产,药用其氯化钠注射液与软胶囊,商品名“恩必普”。丁苯酞研发项目先后被列入国家自然科学基金、“八五”和“九五”国家科技攻关项目。“十五”期间,该项目又被科技部列入国家高技术研究发展计划(863计划)、“创新药物和中药现代化”重大科技专项,其原料药与软胶囊项目获得2009年国家科技进步二等奖。本品于2009年进入国家医保目录。
市场独占情况
虽然丁苯酞是存在于南方泥水匠菜籽中的一种极微量天然单体,而其研发也经历了二十年的漫长历程,但石药集团及其相关企业通过制剂及其制备方法专利,很好地实现并延长了市场独占,其中而“丁苯酞软胶囊及其制备”专利(专利号:200310119336.1)于2012年获得第十三届专利金奖。
目前仅有石药集团恩必普药业有限公司持有丁苯酞及其氯化钠注射与软胶囊剂的生产批文。
市场表现
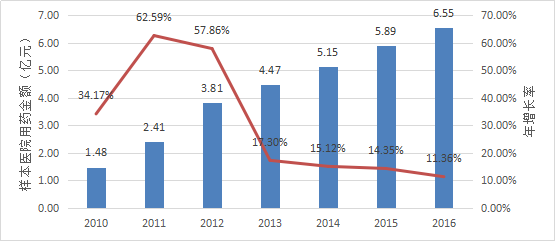
目前,暂时未发现披露丁苯酞整体销售额的数据。根据Pharmarket数据库信息,2016年全国22个重点城市样本医院内丁苯酞的用药金额达6.87亿元,相信其全国整体销售额已经远超10亿元。
丁苯酞的商业成功经历了相对曲折的过程。国内某专业媒体2014年11月发表的《恩必普》一文指出,丁苯酞于2004年取得新药证书并上市以后,由于难进医院主渠道,产品连年亏损,不但新药研发初期国家各部委对丁苯酞投入项目资金难有回报,企业的巨额投入也难以收回,同时还面临着专利期不断荒废的窘境。根据国内22个城市样本医院数据,2005-2009年,丁苯酞市场一趟处于低迷状态,样本医院内用药金额基本维持在200万-600万元之间,五年来未突破千万元大关。2010年起,呈场开始呈迅速上升态势,用药金额从2005年的159万元,增长至2013年的3.3亿元。此8年市场增长210倍,年度复合增长率高达95.0%。
《石家庄日报》2007年12月5日发表的一篇名为《丁苯酞为何“墙内开花墙外香”》一文将丁苯酞上市后早期国内市场的低迷归因于化合物专利的缺失。
3、双环醇
双环醇片,商品名为百赛诺,是我国第一个具有自主知识产权的抗肝炎新药,由中国医学科学院药物所药理学家、中国工程院院士刘耕陶教授及著名药物化学家张纯贞教授合作的科研小组历经15年艰辛研制成功,于2001年9月获新药证书与药品注册文号,持有人为北京协和药厂。此前的2001年2月“抗肝炎新药双环醇的研究”项目获得由科学技术部、财政部、国家发展计划委员会及国家经济贸易委员会联合颁发的“九五”国家重点科技攻关计划优秀科技成果奖,并入选2001年度中国十大医药科技新闻。上市后,双环醇先后荣获2005年北京科技一等奖与国家科技进步奖。
市场独占情况
1988年起,双环醇获得美、欧、日、韩等15个国家与台湾地区的物质发明专利,但由于当时我国的专利法不对药品授予专利权,故未能获得国内专利。中国医学科学院药物研究所针对双环醇申请了一系列外围专利,其中包括“光活双环醇及其制备方法和其药物组合物与用途”(专利号:02156723.9,尚在有效期内),对市场独占权起了一定的保护作用。2009年该专利的专利权人变更为北京协和药厂,目前也只有北京协和药厂一家国内企业持有双环醇及其片剂的生产批文。
市场表现
《河北日报》2014年2月20日发表的一篇名为《十年“冷板凳”只为创新药》一文援引数据称,双环醇上市后当年销售额为8000万元,第三年便超过了1亿元。《科技日报》2016年10月28日发表的《十大科技成就》一文称,独家产品双环醇销售额达30亿元(推测是累积销售额),份额稳居国内口服保肝用药的首位,已在俄罗斯等“一带一路”沿线7国注册上市。
4、异甘草酸镁
异甘草酸镁注射液(商品名“天晴甘美”)是由正大天晴药业利用天然药物甘草有效成分研制的抗肝炎创新药,于2005年9月获得CFDA颁发的新药证书与生产批件。异甘草酸镁是一种全新结构的手性化合物,是甘草酸的单一旋光异构体,具有很强的抗炎、保护肝细胞膜、抗生物氧化等多种药理作用,在药理学及药代动力学等多方面具有突出的优势。临床试验显著其起效迅速,降酶速度和降酶程度均明显高于其他产品,应用范围广,适用于各种肝病的治疗,改善肝功能。异甘草酸镁注射液是国家乙类医保用药。
市场独占情况
正大天晴申请并获得授权的异甘草酸镁化合物专利(专利名称:一种新的化合物异甘草酸镁及其生产方法和用途,专利号:02111693.8)于2007年获得国家专利金奖。目前仅有正大天晴一家企业持有异甘草酸镁及其注射液的生产批文。
市场表现
国内3家媒体报纸于2012年发表文章报道称,2011年异甘草酸镁注射液的销售额达8亿元。
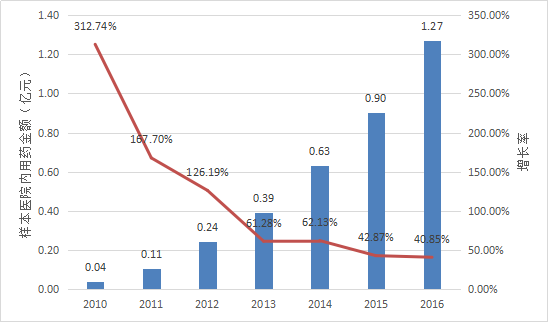
根据Pharmarket数据库信息,2010年以来异甘草酸镁在全国22个重点城市样本医院内用药金额的变化情况如下表所示。
5、艾普拉唑
艾普拉唑是1998年韩国一洋药品株式会社研发的新药,2001年丽珠医药集团与一洋签订关于该品种的《专利许可协议》,取得该产品在中国内地、香港、澳门等地区的独家生产、加工和销售权。虽然是专利许可的品种,但丽珠集团在该品种的投资并不亚于自主研发的品种,集团承诺投资1.156亿元用于建设艾普拉唑原料及制剂的产业化项目。
艾普拉唑于2007年12月获CFDA批准用于治疗胃溃疡等疾病,药用其5mg肠溶片,商品名“壹丽安”。与以往的胃药相比,艾普拉唑具有明显的优势。一是抑制胃酸的活性更强,同等剂量药效高4倍;二是对不同代谢型患者无个体差异;三是毒副反应更少。2017年,艾普拉唑进入国家医保目录。
市场独占情况
如前所述,韩国一洋药品株式会社将艾普拉唑在中国内地等地区的化合物专利权许可给了丽珠集团。
目前仅有丽珠集团一家企业持有艾普拉唑及其肠溶片的生产批文。
市场表现
暂无数据披露了艾普拉唑的整体销售额信息。
根据Pharmarket数据库信息,2010年以来艾普拉唑在全国22个重点城市样本医院内用药金额的变化情况如下表所示。
二.前景可期篇
1、阿帕替尼
阿帕替尼是由江苏恒瑞医药股份有限公司研发的全球第一个在晚期胃癌患者中被证实安全有效的小分子抗血管生成靶向药物,也是晚期胃癌标准化治疗失败后,单独用药疗效最好的药物,同时阿帕替尼是胃癌靶向药物中唯一的一种口服制剂,从而极大了提高了患者的依从性。2014年6月,埃克替尼的临床研究被美国临床肿瘤学会(ACOS)选作大会报告,这是中国创新药研究第一次在全球顶级学术会议上作大会报告,第一次入选该年会优秀研究。根据2015年中国癌症报告,2015年我国预计67.9万例胃癌病例,预期死亡49.8万人。
阿帕替尼片于2014年10月获CFDA批准,药用其甲磺酸盐片剂,商品名艾坦,共有0.25g、0.375g与0.425g三种规格。根据药智网提供的2017年重庆与江西最新的药品招标信息,本品0.25g、0.375g与0.425g规格的单价分别为 215.1元、296.1元与324.64元。
市场独占情况
恒瑞医药申请的第200810149651.1号中国专利保护了阿帕替尼及其甲磺酸盐,该专利已获授权,将于2028年失效。目前仅有恒瑞医药一家企业持有阿帕替尼及其片剂的生产批文。
市场表现
目前暂无数据直接披露阿帕替尼的整体销售额。
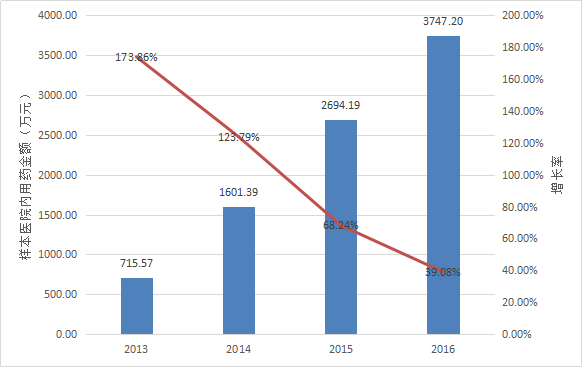
根据Pharmarket数据库信息,2015年与2016年,全国22个重点城市样本医院内阿帕替尼的用药金额分别为5946.85与7860.19万元,2016年较2015年同比增长32.17%。
2、艾拉莫德
艾拉莫德是由天津药物研究院与江苏先声药业有限公司投资数亿元,历时12年而研发成功的我国拥有自主知识产权的全球首个小分子治疗类风湿性关节炎药物,于2011年8月获1类新药证书及药品注册批文,药用其25mg片剂,商品名“艾得辛”,而其上市后研究被纳入科技部“十二五”重大创新科技重大专项支持项目。
中华医学会风湿病学分会主任委员会、北京大学人民医院风湿免疫科主任栗占国于2012年1月接受《健康报》记者采访时表示,类风湿性关节炎是全球致残率最高的疾病之一,在我国约有500万名患者需要治疗。“艾得辛”上市之前,临床使用的药物多为症状治疗,且存在滥用激素、止痛药等不规范治疗的行为,治疗效果也不理想。艾得辛治疗风湿性、类风湿性关节炎,最快4周~6周即可起效,可抑制多种细胞因子和类风湿因子的表达,明显改善类风湿性关节炎患者的症状与体征。此外,艾得辛还能有效阻止骨质破坏,降低患者的致残致畸率。艾拉莫德于2014年被写入亚太抗风湿病联盟的类风湿治疗指南,并于2017年被纳入国家医保。
市场独占情况
目前,仅有先声药业一家企业持有艾拉莫得及其片剂的生产批文。
市场表现
暂无数据披露了艾普拉唑的整体销售额信息。
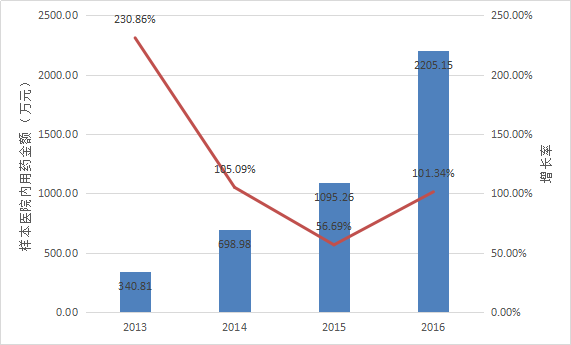
根据Pharmarket数据库信息,近年来艾拉莫德在全国22个重点城市样本医院内用药金额的变化情况如下表所示。
3、艾瑞昔布
艾瑞昔布是江苏恒瑞医药自主研发的1类新药,于2011年5月获批,商品名为“恒扬”,药用其0.1g片剂。艾瑞昔布缓解骨关节炎患者疾病症状的效果及胃肠道安全性特征均与塞来昔布相当,但其心血管、肾脏安全性特征更优。2017年,艾瑞昔布被纳入国家医保。
市场独占情况
目前,仅有恒瑞医药一家企业持有艾瑞昔布及其片剂的生产批文。
市场表现
暂无数据披露了艾普拉唑的整体销售额信息。
根据Pharmarket数据库信息,近年来艾拉莫德在全国22个重点城市样本医院内用药金额的变化情况如下表所示。
三.小结
提到创新药物的研发,大多会用“十年磨一剑”来形容其过程的漫长,然而“剑”磨好后,是“立即露锋芒”还是“锋芒久未露”却受着太多因素的影响。与国外情况一样,除了少数特效药或急需药,大多数创新药从上市到实现“丰厚的商业回报”会经历或长或短的过程。
2000年以后批准上市的国产1类化药新药屈指可数,其上市后市场的表现也各不相同。丁苯酞、双环醇、异甘草酸镁与艾普拉唑均是21世纪第1个10年内批准的新药,在经历了漫长的市场积累后,均已在样本医院内实现了过亿的年度销售额。埃克替尼在上市5年后即已实现了10亿元的销售业绩,的确是国内创新药物前所未有的商业奇迹。而阿帕替尼、艾拉莫德与艾瑞昔布上市较晚,其样本医院内用药金额尚处于千万元级别,但每年均保持着2位以上的增长率,过亿指日可待。
除了本文所述的几种新药,CFDA还于2016年10月批准了泰州复旦张江药业的海姆泊芬及其注射剂用于治疗皮肤病,于2014年2月批准江苏豪森的吗啉硝唑及其氯化钠注射液用于治疗细菌性感染、2013年4月批准广州南药新药的帕拉米韦及其氯化钠注射液用于治疗流感,但上述三种1类化药的市场规模均尚未明朗,故未予以论述。
当然,由于笔者资源与精力的限制,对1类新药品种的搜集以及各品种信息的整理难免有遗漏,还望广大读者朋友不吝指正、补充。
最后,既然本文所述为化药1类新药,不得不说的一个品种就是青蒿素。之所以没有在前文对其进行论述,是因为青蒿素的价值已经大大超出了商业指标所能衡量的范围,它是新中国老一代科学家为世界人民健康事业所做的巨大贡献,也是留给中国新药研发的一笔巨大的精神财富!




 相关新闻
相关新闻