自2015年7月22日以来,自查批次已公布了七个批次,共2033个受理号进入临床自查核查清单目录以内。这七批自查核查清单中,进口药品共387个。国内省份中,江苏、北京、山东、广东和浙江分别列前五位,受理号数都过100个。
自2016年优先审评制度实施以来,截至2017年5月21日,咸达数据V3.2发现,共212个受理号获得优先审评,其中91个已进入临床自查核查,43%的占比可见优先审评的加速力度。2016年临床自查核查清单上的受理号14%是来自优先审评,2017年此比例上升到34%,由此可见第一批自查之后的几批自查产品,更多的是与创新性、临床需求挂钩的项目。
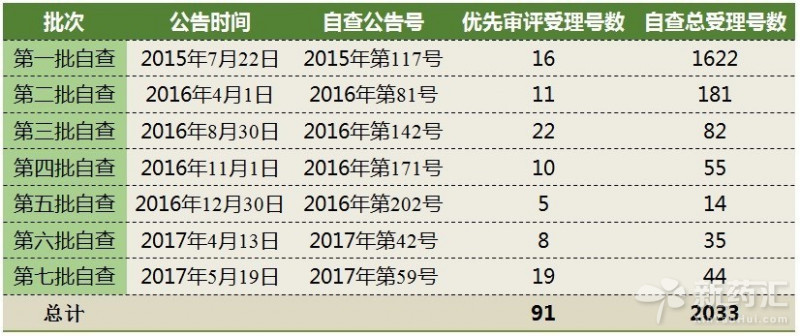
表1 七批自查受理号数
(数据来源:咸达数据V3.2)
国产自查以仿制药为主:石药和天晴是2~7批自查产品数最多的企业
公告撤回基本上只有第一批临床自查核查清单中有所公布。以企业为单位统计第二到七批临床自查核查清单产品,石药集团和正大天晴申报产品数并列第一多。这两家的进入临床核查自查清单的产品主要为仿制药,特别是首仿药或双报药为主。
石药集团申报的有多潘立酮片、盐酸二甲双胍片、盐酸莫西沙星片、注射用紫杉醇(白蛋白结合型)、盐酸决奈达隆片和伊潘立酮片,目前只有盐酸决奈达隆片进入药物临床试验数据现场核查计划公告(第5号)。
石药盐酸二甲双胍片在美国ANDA已获批。CFDA在2017年5月18日终于发布了仿制药质量和疗效一致性评价研制现场核查指导原则等4个指导原则的通告(2017年第77号),包括仿制药质量和疗效一致性评价的“研究现场核查指导原则” “生产现场检查指导原则” “临床试验数据核查指导原则”和“评价有因检查指导原则”,这意味着美国和中国双报的产品有望加快获批,石药的盐酸二甲双胍片有望在2017年内上市。
正大天晴申报的有富马酸替诺福韦二吡呋酯片、来那度胺胶囊、盐酸安罗替尼胶囊、注射用福沙匹坦双葡甲胺、注射用左泮托拉唑钠和瑞舒伐他汀钙片。
国内厂家自查申报也扎堆:氨氯地平热度不减
国内厂家对仿制药申报热度也体现在第二到七批临床自查核查清单产品中。苯磺酸氨氯地平片的国内厂家的生产批文数高达65个,但其依然是国内生产厂家申报最受欢迎的产品,共4家企业申报,分别是重庆药友制药有限责任公司、酒泉大得利制药有限公司、北京永正制药有限责任公司和河北东风药业有限公司。目前只有重庆药友制药有限责任公司在药物临床试验数据现场核查计划公告(第7号)清单上。据悉,重庆药友此项目是按一致性评价的质量标准申报的。
其次就是富马酸替诺福韦二吡呋酯片,正大天晴药业集团股份有限公司、齐鲁制药有限公司和安徽贝克生物制药有限公司仍在等待第二家国内厂家上市的机会,三家都在药物临床试验数据现场核查计划公告中,按理应在2017年有审批结果。2016年成都倍特药业有限公司上市该品种,当时获批的适应症为HIV-1感染,富马酸替诺福韦二吡呋酯适用于与其他抗逆转录病毒药物联用治疗成人HIV-1感染。
然而,总局关于鼓励药品医疗器械创新保护创新者权益的相关政策(征求意见稿)曾提到,“挑战专利成功和境外已上市但境内首仿上市的药品给予1.5年数据保护期,在数据保护期内,审评机构不再批准其他申请人同品种上市申请,申请人自行取得的数据除外”。成都倍特药业有限公司首仿上市时间是2016年11月,富马酸替诺福韦二吡呋酯片第二家是否就此顺延到2018年6月上市,拭目以待。
2017年广生堂富马酸替诺福韦二吡呋酯胶囊获批,从CDE临床试验可见,广生堂的适应症为用于治疗慢性乙型肝炎的成年患者。福建广生堂药业股份有限公司共有2个受理号进入第一批临床自查核查,旧化学药分类5类申报的CXHS1300370在公告2015年第264号撤回,旧化学药分类3.1类申报的CXHS1400157则没有撤回且获得优先审评。目前富马酸替诺福韦二吡呋酯胶囊在申报的有成都倍特药业有限公司。
盐酸莫西沙星片同样也是热点,北大医药股份有限公司、石药集团欧意药业有限公司和南京新港医药有限公司在临床自查核查清单之中,但尚无一进入药物临床试验数据现场核查计划公告。
进口药上市又快又新:诺华沙库巴曲缬沙坦钠片(LCZ696)即将获批
自总局2017年3月17日公开征求“关于调整进口药品注册管理有关事项的决定(征求意见稿)”意见以来,进口产品利好消息不断。第七批自查中44个受理号数中就有35个受理号来自进口产品。第七批自查获得优先审评资质的7个产品19个受理号只有盐酸安罗替尼胶囊是国内生产厂家正大天晴药业集团股份有限公司,其余都是进口产品。
7个优先审评的产品中,勃林格殷格翰(中国)投资有限公司的噻托溴铵奥达特罗吸入喷雾剂和拜耳医药保健有限公司的注射用重组人凝血因子Ⅷ申报的是临床,其余都是申报上市,这意味着5个产品有望在2017年获批。
正大天晴盐酸安罗替尼胶囊目前已完成临床适应症有三线及以上晚期非小细胞肺癌,在研究的适应症有晚期甲状腺髓样癌、晚期软组织肉瘤、结直肠癌、晚期肾细胞癌、晚期胃癌、胃食管结合部腺癌和食管鳞癌。奥达特罗吸入喷雾剂适应症为慢性阻塞性肺病(COPD)患者。德拉马尼片治疗多药耐药结核病。灵北抗抑郁药氢溴酸伏硫西汀片用于重度抑郁症(MDD)成人患者的治疗。诺华的沙库巴曲缬沙坦钠片(LCZ696)临床试验已完成评价LCZ696用于原发性高血压治疗8周后的疗效和安全性,以及降低慢性心力衰竭的发病率和死亡率的研究,预计适应症为慢性心力衰竭。
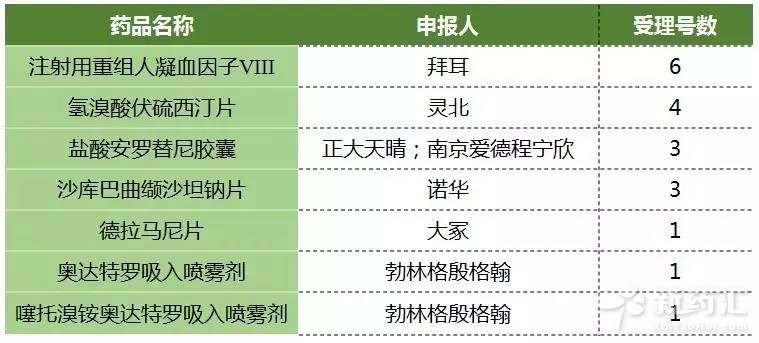
表2 第七批自查优先审评产品
(数据来源:咸达数据V3.2)
焦点<<<
进口药已经提速,
国产药审批是否也能提速?
一般而言,进入临床自查核查清单、进入临床试验数据现场核查计划公告后才进入药品审批流程,第二批自查名单至第七批自查名单国产厂家受理号数195个,优先审评仅12个,进入临床试验数据现场核查计划公告25个;相比较而言,进口产品受理号216个,优先审评63个,进入临床试验数据现场核查计划公告96个。
优先审评比较的是临床需求和创新性,我国申报的主要仿制药为主,国产药品的优先审评数量较低是意料之中。但是,从进入临床试验数据现场核查计划公告的进度来看,国产产品的审批进度低于进口产品。
不少进口药企在抱怨2017年药政不利过期原研药,过期原研药医院市场丢标严重,2017年进口新药的获批或许可暂时缓解进口药产品线青黄不接的困境。
国内生产厂家面临同样困境。不幸的是,许多厂家手里没有符合改革新规要求的项目。被第一批自查核查耽误没上市且对项目质量有自信的仿制药项目翘首以待更快的审批速度,2015年至今已两年。“去”,或是“留”,亟需定锤之音。




 相关新闻
相关新闻