CDE公布评定原则10种儿童药优先审评审批
12月21日,为贯彻落实《关于药品注册审评审批若干政策的公告》(2015年第230号)要求,国家食品药品监督管理总局药品审评中心(CDE)公布《临床急需儿童用药申请优先审评审批品种评定的基本原则》,并根据上述原则对10种儿童用药优先审评申请进行了评定,公示日期为:2015年12月21日-2015年12月28日。
《基本原则》中对新药、改剂型或新增规格的、
仿制药三种类型制定了不同的评定基本原则。
其中,新药申请应该满足以下任一条件:1、针对严重威胁儿童生命或者影响儿童生长发育,且目前无有效治疗药物或治疗手段的疾病的申请;2、相比现有的治疗手段,具有明显治疗优势的申请。
改剂型或新增规格的儿童用药申请应同时满足以下两个条件:1、现有的药品说明书中包含有确定的“儿童用法用量”的申请;2、现行的剂型或规格均不适用于儿童,新增的剂型或规格适合于儿童的申请。
仿制药申请方面,对于目前市场短缺的儿童用药品,实行优先审评。仿制申报厂家的数目为多家申请的,按照申请先后排队顺序,对排第一位的优先审评,若经审评不符合要求,则取消优先资格,后面的同品种申请可按序增补替代。
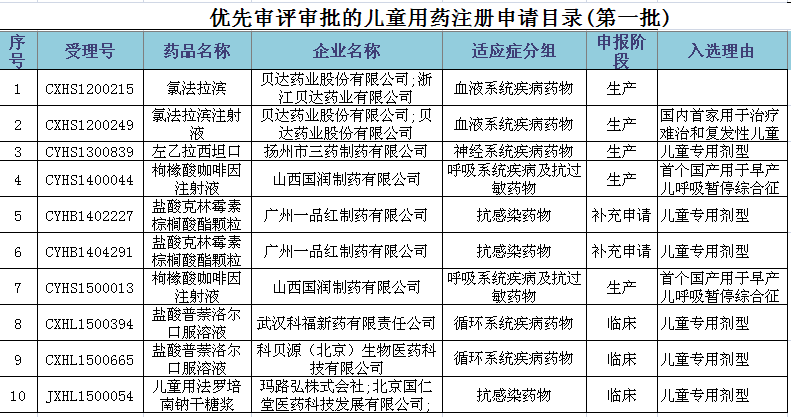
优先审评审批的儿童用药注册申请目录(第一批)

分享到:





 相关新闻
相关新闻