编者引言
ELISA这项经典技术已拥有多年的发展历史,有多种方法类型,竞争性ELISA技术就是其中一个基本类型,它同夹心ELISA法技术一样,也被应用到药物PK分析研究中;如何基于竞争性ELISA原理构建好一个竞争性 Assay并在方法建立实践中把握好相关要点,对整个方法的最终成功尤为重要。作者结合自身实践体会与案例以此文略作阐述,供大家参考。
ELISA技术自从上世纪70年代提出以来,经过几十年的发展,业已成为生物医药研发领域不可或缺的经典技术。ELISA方法有各种不同类型的分类形式,基于反应原理和模式可主要分为直接法、间接法、夹心法及竞争法,其它基于不同的分子标记形式、载体形式、捕获形式或信号产生形式等等的方法如荧光法、化学发光法、电化学发光法、类芯片法、微球法都是这4种基本方法的组合或衍生。
其中,夹心法在大分子药物如抗体、蛋白药物的PK分析领域里得到了广泛应用。而对于小分子化合物或分子量偏小的多肽药物,除了LC-MS/MS可进行它们的PK分析外,竞争性ELISA方法也可以发挥其特有的应用价值和优势。不仅如此,即使是分子量较大的蛋白及抗体在实践中也仍然可以考虑采用竞争性ELISA法进行相关的PK分析。因此,从可被应用的药物分子类型广度看,竞争法是在药物PK分析领域中最具使用潜能的一种ELISA方法。
迄今数量繁多的现代药物中,小分子药物占据着绝大多数,许多小分子化合物是不具免疫原性但具免疫反应性的半抗原,如常与大分子抗体偶联的作为ADC的Payload的细胞毒素,部分激素等。
多肽也是现代药物中举足轻重的一部分,例如常见部分激素药物为多肽,另如肿瘤新生抗原肽近年还成为药物开发的一个热点。多肽分子量相对于化合物而言比较大,相对于抗体、重组蛋白或融合蛋白,其分子量则又很小,往往缺乏较为复杂的二级结构或空间结构等,免疫原性较弱,是类半抗原物质。这些半抗原或类半抗原分子在理论上自身单独不能或难以刺激机体产生抗体,但在偶联了载体抗原分子后再免疫动物可以制备出与该分子本身进行结合反应的抗体,从而为构建对其进行ELISA测定的方法提供工具性试剂。
这些半抗原分子很小,往往其实仅有一个表位,不能形成不同位点与抗体结合的夹心之式;即使有的类半抗原多肽可能会存在两个或以上的表位,但抗体制备中的现实是常很难获得针对不同表位可以构成夹心配对使用的抗体,此种情况下,选择构建竞争性ELISA方法则是一个因材施措的策略。有些分子量足较大、足够复杂的含有多个表位的具完全抗原性的分子,如在仅一株单抗或仅有其多抗可被利用的实际条件下,也需考虑选择设计竞争性的检测方法;当然,对于具备条件采用夹心法检测的完全免抗原性抗体或蛋白分子,有的情况下相关研究人员仍考虑使用竞争性ELISA方法进行测定也不是未尝不可。
如何基于自己可利用的抗体试剂实际情况、所在实验室具体的平台条件,综合评估目标研究的试验设计,基于竞争性ELISA原理成功建立一个 “Fit-for-Purpose”的分析方法,也是临床前和临床PK或PK/PD评价研究中一个具体又现实的技术性问题。
竞争性ELISA原理用于药物PK定量分析的方法学设计策略
用于定量分析药物PK浓度的竞争性ELISA方法通常有两种基本的Assay构建模式:
一种模式是以单抗或多抗作为固相捕获试剂,样品中游离(本文中游离特指非固相化)药物与标记药物竞争结合固相的抗体,如游离药物和生物素标记的药物竞争性结合包被在板孔的抗体(参见图1)。
另一种模式就是将一定浓度的药物包被在固相载体上,采用样品中游离药物与固相药物竞争性结合游离的抗体(若图2)。
这两种Assay模式在抗体药PK分析的应用上也可以转化为游离药物与标记药物竞争它们固相的靶点分子,或游离药物与固相药物竞争性结合标记的靶点分子;对于有的药物也还可以转化为对其受体分子的竞争性结合。具体设计时可以基于此两种Assay模式进行衍生或转化。
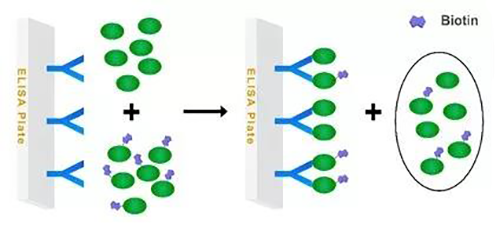
图1 游离药物与标记药物竞争的Assay模式
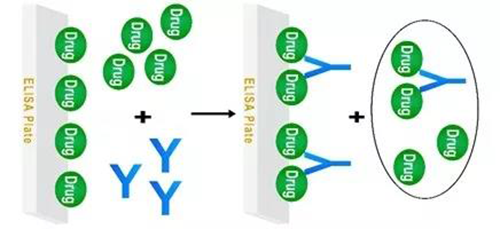
图2 游离药物与固相药物竞争的Assay模式
基于药物与标记药物竞争的这一模式,药物分子可以用辣根过氧化物酶(HRP)或碱性磷酸酶(AP)直接标记,这样的标记的药物主要用于对灵敏度要求不高且基于传统可见光吸收法检测平台的竞争性Assay开发。基于传统光吸收检测平台也可以采用生物素标记,借助链霉亲和素-生物素信号放大系统进行较高灵敏度Assay的构建。随着分子标记技术的发展和新平台的不断出现,如若需要开发更为灵敏的竞争性Assay,也可以采用荧光素标记药物分子建立荧光检测的方法,或可采用镧系元素中的Eu(铕)标记药物基于时间分辨荧光平台进行检测,如有MSD平台的分析实验室还可以利用该公司的SULFO-TAG标记药物分子开发电化学发光的检测方法。采用标记药物和非标记药物竞争的模式,选择什么样的标记分子,产生什么类型的信号,可以基于自身实验室平台条件或仪器所拥有的检测功能模块和实际需要的灵敏度及标记的可行性情况实施具体的策略。
采用游离药物与固相药物竞争的模式时,一个优势是通常可以免除进行分子标记的麻烦,节约了标记成本,特别是当标记缺乏可行性时,如有些药物分子缺乏与标记物相结合的基团或药物分子被标记后其本身的稳定性或其它基团受到了影响的情况下采用此种竞争法是一种很好的应对策略。然而,有时实践中我们会发现药物直接包被在固相载体上限制了其与非固相抗体的有效结合,Assay的整体信号不容易上去,灵敏度难得到提高等现象,可能是固相化后其表位受到了影响。然而,将非标记的药物直接固相化改造为间接固相化,这种结合反应被影响的情况有时会得到改善,如在标记可行的情况下,先将药物进行生物素标记,使生物素标记的药物与固相载体上包被的Streptavidin结合间接实现药物固相化再与游离药物竞争(参见图3)。分析人员可以自行包被Streptavidin,也可以购买商业化的包被有Streptavidin材料直接利用,如Thermo和MSD等公司均有商业化的Streptavidin Coated Plate提供。
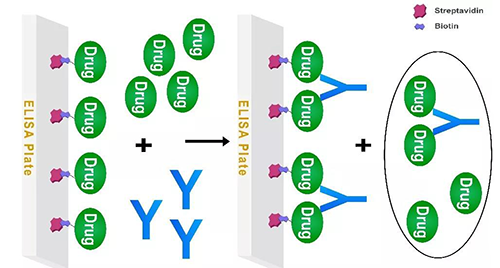
图3 游离药物与间接固相化药物竞争的Assay模式
分析方法学模式的构建要结合具体实验室的平台条件、可供利用的抗体情况、药物分子的结构与性质、目标研究对灵敏度和方法检测范围的适用性要求等因素来制定具体策略。
竞争性ELISA原理应用于药物PK分析方法学建立的实践性要点
竞争性反应体系的构成
竞争性Assay的一个核心原理就是“竞争”,因此实践此类方法建立的核心要点就是具有竞争性特征的抗原抗体反应体系的构成,即是要营造一个能促成“竞争”产生的ELISA反应系统。上述两种基本的竞争性ELISA Assay Format,都由三个主要成分构成,即:游离药物、标记药物或固相化药物、抗体。这三大主要成分,我们可以分别把其概念化为:竞争因子、被竞争因子、资源因子。
这三大因子是构成竞争性环境即反应体系的必需。标记药物或固相化于载体的药物在反应体系中浓度是固定的;而样品中游离药物浓度是非固定的,特别是PK定量分析方法中要用到标准曲线,被测样品中游离药物与构成标准曲线的不同浓度梯度的游离药物都是要与标记药物或固相化于载体的药物竞争性结合体系中的抗体,因此反应体系中抗体可以说是竞争性Assay中的“资源因子”;游离药物与标记药物或固相化于载体的药物互为竞争和被竞争的关系,为便于阐述,此文中我们把游离药物称为“竞争因子”、标记药物或固相化于载体的药物称为“被竞争因子”,其实两者互为彼此的竞争因子。
营造竞争性反应体系的基础
在微观世界里的一些分子间的相互影响或作用其实与宏观世界甚至人类世界里的现象是具有共通的地方,在某种资源有限的情况下,人与人间就会发生对该有限资源的争抢即竞争性地占有资源。同样,竞争性Assay反应系统中竞争因子与被竞争因子间的竞争关系发生基础就是“资源有限”,对于竞争性ELISA而言就是抗体有限或具体说抗体所含的药物总结合位点有限。如果抗体量过多或所谓饱和,则不能造成游离药物与标记药物或固相化药物的竞争,这样的竞争性ELISA反应系统则是失灵的。
表1和图4为一个正在建立中的某低分子药物的竞争性ELISA PK Assay案例(案例一),根据给药剂量、方式等预测需要开发一个定量范围在0.391-25ng/mL的分析方法,采用的是固相药物和游离药物竞争性结合其单克隆抗体的模式。同一批配制来源的标准曲线,当抗体浓度(此处以实际使用时的稀释倍数显示)非常高时(1/500),不同浓度的标准品的信号值无梯度性变化和明显差异,此情况下,抗体浓度过高没有造成游离药物竞争干扰掉固相药物与抗体的结合而不能使信号呈浓度梯度依赖性的差异变化。其它条件都相同时,降低单抗稀释倍数到1:2000,标曲高浓度点间不同浓度梯度的标准品的信号值差异开始明显呈现,预示竞争产生;当继续降低单抗稀释倍数至1:5000,这种浓度梯度依赖性的信号差异则更为显著,标曲拟合趋势向好。
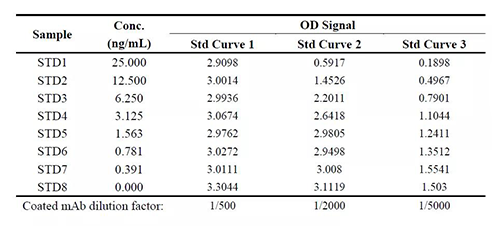
表1:案例一中调节固相化抗体浓度后对方法表现的影响
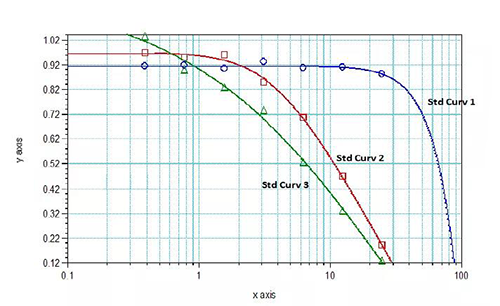
图4:表1对应的3个不同条件下的标准曲线
竞争因子间的调控
对于一个竞争性ELISA Assay而言,除了仅提供有限的“资源因子”,还需考虑到“竞争因子”与“被竞争因子”间的势力大小问题,即互为竞争对象的两者间不能出现竞争绝对势力方。绝对势力方会因其绝对优势而导致对应的竞争方毫无对其干扰的能力。对于这一点人类世界的现象和微观世界的现象同样是相通的。如两个势均力敌的人搏斗时可以僵持很久,当一个人与两个人同时搏斗时也可能会坚持一段时间,当一个人同十几个人同时搏斗时因为力量对比悬殊,毫无对抗能力可言,极易瞬间被对方击溃,甚至连出招抵抗的机会都没有。竞争性ELISA方法建立时,如果作为被竞争因子的固相化药物或标记药物比例或浓度过高,则导致作为“竞争因子”的游离药物不会或几乎不会对被竞争因子与抗体结合的干扰,标准曲线的不同浓度标准品间的信号梯度不能出现或不显著,标准曲线难以拟合或拟合质量不高而不具备较好的对未知样品的测量分辨力,进而影响对实际的样品真实准确定量。因此,实践中客服这一问题时要注意参与反应的竞争因子间比例调控。
观察竞争性因子的竞争能力,可以通过将样品信号值归一化为结合百分比(B/B0)来观察,则竞争因子干扰被竞争因子与抗体结合能力更显直观。实践中常见的就是仅在几个高浓度标曲点上出现了结合百分比的梯度依赖性差异,低浓度点的B/B0无显著差异或几乎不变,即低浓度标准品不能很好地参与标曲拟合,此种情况下一般是被竞争性因子相对于低浓度游离药物而言仍占据了绝对优势,从而影响了方法的检测灵敏度,可以尝试调低被竞争因子的使用浓度或比例。如表2和图5所示案例二:该方法为一个抗体药物的竞争性ELISA方法,Assay Format为游离药物与生物素标记药物竞争其抗独特型抗体,同一批配制来源的标曲,在生物素标记药物稀释比例为1/30000时,几个高浓度标曲点上出现了结合百分比的浓度梯度依赖性差异,但低浓度水平的标准品B/B0几乎无差异,标曲低浓度端趋平缓,拟合不理想,其低浓度质控品的准确度也受到影响;当生物素标记药物稀释比例为1/40000时,低浓度水平的标准品B/B0差异显著,标曲得到了很好拟合,来自于同一配制的低浓度质控品的准确度也趋好。
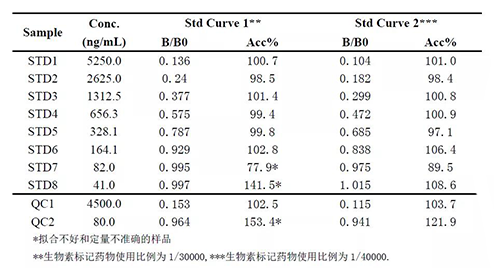
表2:案例二中不同生物素标记药物比例下的方法表现的比较
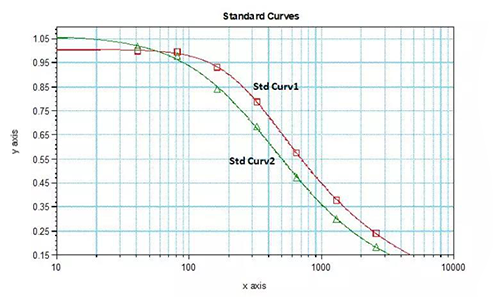
图5:表2对应的2个不同条件下的标准曲线
平衡性竞争体系与非平衡性竞争体系的应用
在社会生活中,我们经常听说不对等竞争或不公平竞争。竞争性ELISA Assay同样可以有对等的竞争和不对等的竞争,此文将其概念化为平衡竞争法和非平衡竞争法。
平衡竞争法中是同步开启“竞争因子”与“被竞争因子”对“资源因子”如抗体的结合反应,在标记药物与非标记药物的竞争性Assay Format中,将标记药物与非标记药物同步或几乎无时差性加入到已包被有抗体的固相载体中实现平衡的竞争;在游离药物与固相药物的竞争性Assay Format中,先将含游离药物的样品加入已包被药物的固相载体中,再行加入抗体实现平衡的竞争。
反之,非平衡竞争法中则是非同步开启“竞争因子”与“被竞争因子”对“资源因子”如抗体的结合反应;在标记药物与非标记药物的竞争性Assay Format中,可以先将标记药物或非标记药物加入到已包被有抗体的固相载体中,反应一段时间后再加入另一非标记药物或标记药物实现非平衡式竞争;在游离药物与固相药物的竞争性AssayFormat中,先将含游离药物的样品与抗体在单独的载体中混合反应一段时间后,再加入到已包被药物的固相载体中,或先将抗体加入到已包被药物的固相载体上,反应一段时间后,再将含游离药物的样品加入其中参与反应实现非平衡式竞争。一般来说,研究人员习惯于平衡性竞争法的操作流程,但有的情况下采取非平衡的竞争法,有利于Assay性能的优化。
如表3和图6中的案例三,采用的是固相抗原和游离抗原竞争性结合抗体的模式定量检测某多肽药物,此例中的标曲与QC也来源于同一批配制。其它条件都相同的前提下,当将游离药物与抗体先混合一起反应一段时间后加入包被有药物的微孔板中,则该分析方法的表现要比先将游离药物加入包被有药物的微孔板中再立即加入抗体的平衡性竞争方式好很多。非平衡性竞争法中的标曲低浓度点间的B/B0间差异更为显著,标准曲线拟合质量更佳,QC的准确度可靠,而非平衡性竞争中不仅标曲低浓度端平缓,同样来源的QC也表现不佳。
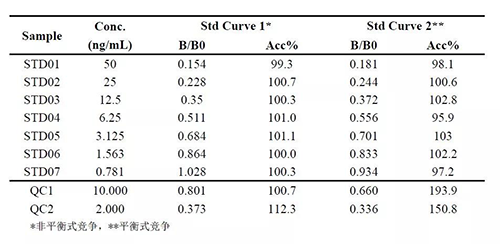
表3 案例三中平衡性竞争与非平衡性竞争的比较
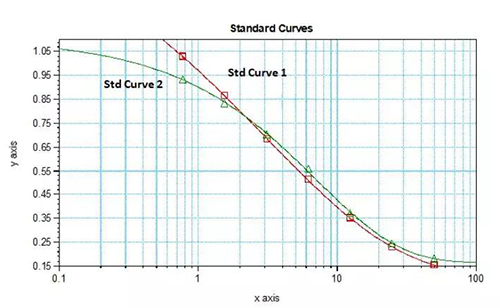
图6:表3对应的2个不同条件下的标准曲线
结语
综上所述,竞争性ELISA法用于PK定量分析是相对较难的一种方法,具体实践中若要利用好这一方法,始终要基于“竞争”这一根本原理展开反应体系的构建与优化。由于分子间的竞争与相互作用,都是肉眼无法看到的微观世界里的行为,将宏观世界或说人类世界的现象发散到对微观世界中个体间关系和作用的想象与思考中,未免不是一个借鉴性思维方式。同人类世界相似,实践中无论是基于哪种竞争性分析模式,首先要营造好竞争性的环境,即提供有限的资源引发竞争;还要促进差异化的“竞争”效果的产生,对于竞争性ELISA方法,竞争性因子间无需势均力敌,但要防止具有绝对优势的竞争因子出现。为便于阐述,上述内容主要基于传统的竞争ELISA检测模式进行了举例和阐述,文中这些实践性的策略和要点可以结合一些新的平台进行衍生和优化使用,并也可以拓展到对内源性分子的检测中,笔者的实验室都有着各种衍生性的竞争性ELISA方法的具体实践,原理相通,不再一一举例。此外,作为PK定量的ELISA方法同常用到的其它PK定量法一样,方法建立后也需要进行各种后续参数的优化与验证,已有很多相关文献阐述,因此本文不再赘述,把握好本文提出的策略和要点,将会为后续各参数的顺利优化和验证奠定一个良好基础。
(未经许可,文章内的所有图片和数据不得引用)
作者简介
章登吉,本硕博分别就读于安徽师范大学、上海师范大学&中国农业科学院上海兽医所和复旦大学,主攻方向为大分子药物与细胞基因治疗药物的分析与评价。曾任职上海药明康德大分子生物分析部多年,加入美迪西后创建了生物技术药物分析团队,现为美迪西普亚生物技术药物生物分析部门负责人,具有13年多的临床和临床前生物技术药物分析经验,负责过Novartis, Pfizer, Lilly, J&J, Genentech, Medimmune, Takeda,石药集团等多家医药企业的多类型生物药相关分析评价工作。在生物技术药的药代动力学、毒代动力学、免疫原性及生物标志物相关的分析方面有着丰富的理论基础和实践经验,撰写相关文章多篇,作为第一发明人申请相关国家发明专利五项,有三项已经获得授权。
实验室简介
美迪西生物技术药物的生物分析实验室拥有SpectraMaxM4/M5/i3x, MSD S600, Luminex, Biacore 8K, Envision, Gyrolab,Covaris E220R, ABI7500 qPCR仪等全方位多功能的技术平台,提供全面符合FDA/CFDA GLP,GCP规范的生物技术药物生物分析服务,以支持蛋白药物、抗体药物、ADC药物、多肽药物、核酸药物、细胞基因治疗药物的早期筛选与开发,及其临床前和临床相关研究。
关于美迪西
美迪西(股票代码:688202)是一家药物研发外包服务公司(CRO),在上海建立了一家集化合物合成、化合物活性筛选、结构生物学、药效学评价、药代动力学评价、毒理学评价、制剂研究和新药注册为一体的符合国际标准的综合技术服务平台,并得到了国际药品管理部门的认可。美迪西普亚的动物实验设施获得AAALAC(国际动物评估与认证协会)认证和国家药品监督管理局NMPA GLP证书,并已达到美国食品药品管理局GLP标准。
美迪西拥有丰富的全球合作经验,2015年以来,美迪西在全球服务超过500家活跃客户,已为武田制药、强生制药、葛兰素史克、罗氏制药等多家全球性制药公司及恒瑞医药、扬子江药业、石药集团、华海药业、众生药业等国内外知名客户提供研发外包服务。
联系我们
Email: marketing@medicilon.com.cn
电话: +86 (21) 5859-1500(总机)





















 相关新闻
相关新闻