肥胖和代谢综合征人数在全世界范围内迅速增长,并会导致高发病率和死亡率。医疗界一直在重点关注着肥胖及其并发症的发展预防和治疗策略。在哺乳动物中,棕色脂肪组织(BAT)和白色脂肪组织(WAT)均可促进全身能量稳态,但是它们的解剖结构、形态和功能却大不相同。
BAT的激活增加能量消耗,它的活性与身体质量指数和脂肪量成反比,这使得BAT有望成为一个抗肥胖治疗剂。BAT由于其独特的解偶联蛋白1(UCP1)表达而产生热量,该蛋白通过将质子动力与三磷酸腺苷的产生解偶联来耗散能量。尽管UCP1的表达在基础条件下仅限于BAT,但长时间的冷暴露或β3-肾上腺素刺激不仅可以增加BAT中UCP1介导的产热能力,还可以激活WAT中褐色样米色脂肪细胞的聚集。在成人中,WAT分布在全身并位于浅层脂肪垫上;但BAT存在于深层脂肪垫的较小区域,例如子宫颈、锁骨上和椎旁区域。考虑到其丰富性和特殊位置,WAT更容易获得和操纵。WAT诱导的褐变可能具有预防或治疗肥胖症和与肥胖相关的代谢异常的巨大潜力。
在先前的研究中已经表明,小鼠UCP1的异位表达可以使骨骼肌和脂肪组织免受饮食诱导的肥胖,猪缺乏功能性的UCP1基因,而白色脂肪中UCP1的异位表达促进了脂解和耐寒性。这些研究清楚地证明了异位过表达的UCP1在动物中的抗肥胖作用。然而,尚不清楚通过激活内源性UCP1基因座位能否在人类中重现这些作用。
自体细胞疗法是一种优选的治疗干预措施,其中将细胞取自个体并施用于同一个体以使免疫排斥最小。自体细胞疗法一直是非常活跃的研究领域,如CRISPR。CRISPR-Cas9系统为哺乳动物细胞中的基因组编辑提供了强大的手段,并且已经在CRISPR-Cas9的基础上开发了几种新工具来实现基因表达的靶向抑制或激活。在CRISPR激活技术中,将核酸酶失活的Cas9与反式激活域融合,并由靶向特定启动子的单向导RNA指导,该合成转录复合物可以激活内源基因的表达。CRISPR激活系统已被用于驱动各种小鼠和人类细胞类型的分化、转分化和重编程。然而,尚未测试过CRISPR工程改造的细胞对全身代谢的影响及其对抗肥胖和与肥胖相关疾病的治疗潜力。
CRISPR激活的高级版本之一是协同激活介体(SAM)系统,其中dCas9与融合蛋白结合,该融合蛋白由来自激活B细胞核因子κ轻链增强子(NF-κB)的两个转录激活域组成和热休克因子1(HSF1)协同促进转录。近日,研究人员在人类白色前脂肪细胞中使用了CRISPR-SAM系统来激活UCP1基因表达。除了表征这些CRISPR工程化的人类细胞外,还通过治疗小鼠的肥胖症和代谢紊乱证明了这些细胞的治疗潜力。该项研究成果发表在《Science Translational Medicine》上。

CRISPR-SAM对UCP1的内源性激活触发了人类白色脂肪细胞中的褐色样表型
研究人员采用了CRISPR-SAM系统来增加人类白色前脂肪细胞中内源性UCP1的表达,共设计了四种不同的指导RNA靶向人类UCP1上游约50至150bp基因和稳定表达的编码dCas9的载体与病毒蛋白转录激活子的四个串联重复序列融合。将CRISPR-SAM系统与gRNA A到D的慢病毒转导到源自两个受试者的人类白色前脂肪细胞中。gRNA-A使UCP1 mRNA 增加约6000倍,使UCP1蛋白增加约20倍。这些发现表明,将靶向UCP1的 CRISPR-SAM和sgRNA结合使用,可以通过开启内源性UCP1表达将人的白色前脂肪细胞改造成人的褐色样细胞。
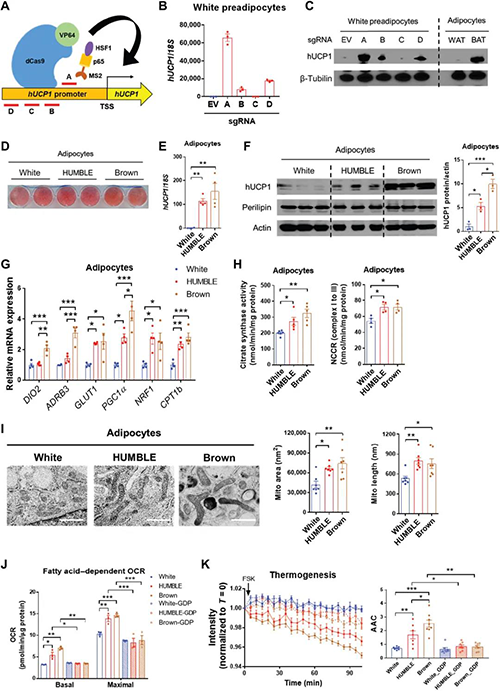
与缺少sgRNA的原始人类白色脂肪细胞相比,HUMBLE细胞在成脂分化后保持了较高的UCP1表达。然而,UCP1在HUMBLE细胞中的表达略低于同一个人的分化棕色脂肪细胞。与白色对照组脂肪细胞相比,HUMBLE细胞显示出升高的GLUT1 mRNA。与棕色对照脂肪细胞相比,HUMBLE细胞导致线粒体活性和线粒体DNA含量增加。与白色对照脂肪细胞相比,HUMBLE细胞显示出更细长且连接的线粒体网络,类似于棕色对照脂肪细胞的线粒体形态。
除了具有棕色对照脂肪细胞的分子和结构特征外,HUMBLE细胞还获得了棕色脂肪样功能性表型。与白色对照组细胞相比,HUMBLE脂肪细胞使用葡萄糖作为底物时,其葡萄糖摄取量、基础呼吸频率、质子泄漏和福司可林(FSK)依赖性耗氧率(OCR)增加。与白色对照组细胞相比,它们还具有更高的脂肪酸依赖性OCR能力,而脂肪酸的摄取没有改变。使用热敏荧光染料,研究人员直接测量了培养细胞产生的热量,发现与福司柯林相比,HUMBLE细胞比白色对照细胞产生更多的热量。这些发现表明,HUMBLE细胞在使用葡萄糖或脂肪酸作为燃料来源方面具有热学能力。
HUMBLE细胞重构小鼠的功能性脂肪细胞
来源:Science Advances
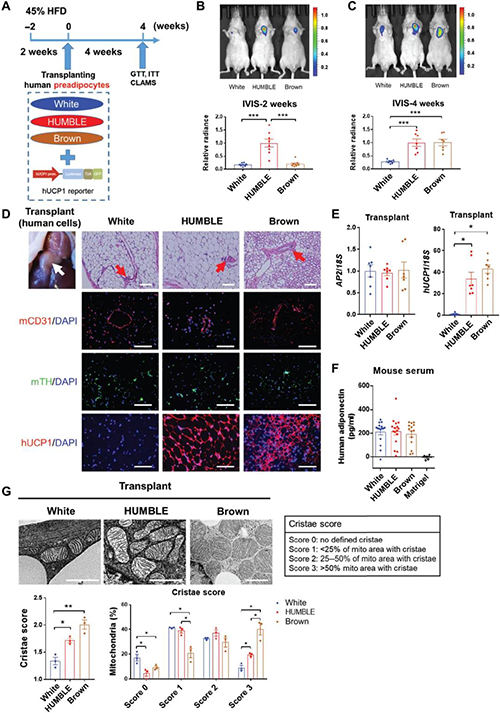
基因工程或药理诱导的米色/棕褐色细胞的移植可改善小鼠体内的代谢稳态。为了确定HUMBLE细胞在体内的代谢影响,将白色对照、HUMBLE和棕色对照前脂肪细胞与Matrigel混合,然后移植到免疫功能低下的裸鼠的胸骨区域。移植后2周,HUMBLE细胞在三种移植细胞系中显示出最高的萤光素酶信号。到第4周在棕色对照细胞和HUMBLE细胞中都检测到大量的UCP1表达,这表明棕色对照前脂肪细胞已分化为成熟的脂肪细胞,且UCP1表达上调。另外,分别通过小鼠CD31和酪氨酸羟化酶的阳性染色所示,移植的组织变得血管化和受神经支配。研究人员在小鼠血清中检测到人脂联素,这表明这些移植物具有可以作为内分泌组织分泌脂联素或其他因子进入循环系统的功能。总之这些数据表明,移植的前脂肪细胞可以在体内重构脂肪组织,从而在体外概括这些细胞的表型。
HUMBLE细胞促进小鼠葡萄糖代谢和生热
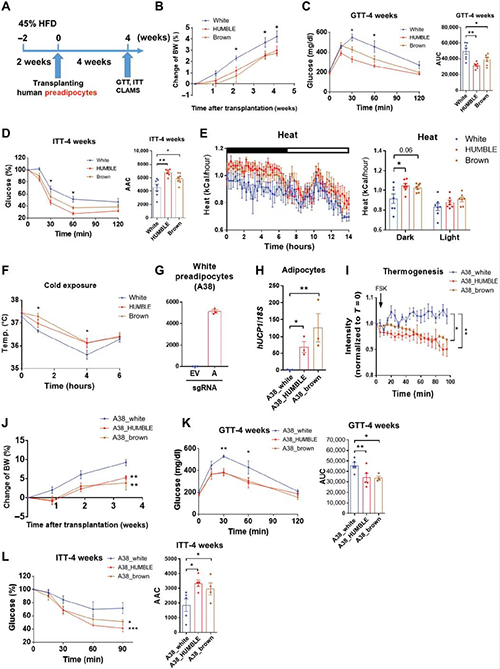
为了研究HUMBLE细胞是否能预防小鼠DIO代谢紊乱,研究人员监测了移植前2周接受45%高脂饮食(HFD)喂养的受体小鼠的代谢表型。接受HUMBLE和棕色对照脂肪细胞的小鼠比接受白色对照细胞的小鼠体重减轻。与接受白色对照细胞的小鼠相比,使用HUMBLE或棕色对照细胞移植的小鼠的葡萄糖耐量和胰岛素敏感性也提高了约30%至35%。血清胰岛素没有统计学上的显著变化。然而,与接受白色对照细胞的小鼠相比,在HUMBLE和棕色对照细胞组中循环甘油三酸酯的浓度降低了。与接受白色对照细胞移植的小鼠相比,棕色对照脂肪细胞移植使小鼠在冷暴露时能够保持更高的核心体温。
来源:Science Advances
为了进一步验证HUMBLE细胞在体外和体内的代谢作用,研究人员使用从另一个个体和相同的CRISPR-SAM系统分离的白色前脂肪细胞生成了另外的HUMBLE细胞系。与上述对供体A41产生的细胞的保护作用一致,由供体A38产生的HUMBLE细胞在体外也显示出很高的产热潜力,并且当使用相同方案进行体内移植时,其糖耐量、胰岛素敏感性和糖耐量均得到改善。这些结果表明基于CRISPR的HUMBLE细胞策略适用于不同的人类受试者。
巨大的细胞移植改善饮食诱发的肥胖小鼠的新陈代谢
来源:Science Advances
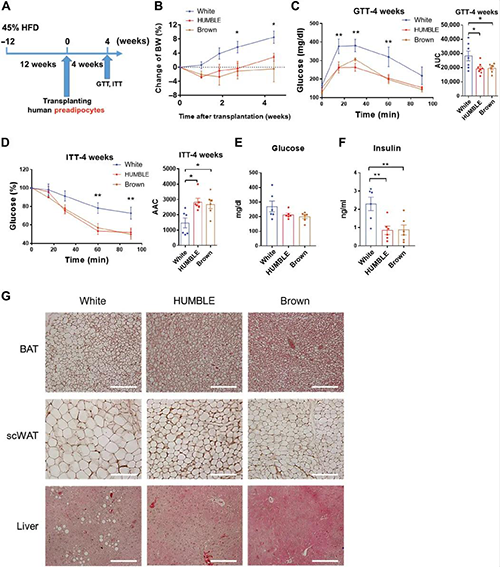
为了检查使用HUMBLE细胞治疗肥胖症的潜力,研究人员将细胞移植到DIO裸鼠中。移植了HUMBLE或棕色对照细胞的DIO小鼠的体重比移植了白色对照细胞的小鼠轻,这与葡萄糖耐量和胰岛素敏感性的显著提高以及移植后4周的循环胰岛素浓度降低有关。与移植了白色对照细胞的小鼠相比,移植了HUMBLE或棕色对照细胞的小鼠的肝脏脂质含量降低了,内源性BAT和皮下WAT中的脂质滴大小相应降低了。总之,这些数据表明,HUMBLE细胞移植可能是潜在的抗肥胖治疗策略。
HUMBLE细胞移植在体内激活内源性鼠BAT

来源:Science Advances
与具有白色对照细胞移植的小鼠相比,接受HUMBLE或棕色对照细胞的小鼠从循环中清除葡萄糖放射性示踪剂的速度更快,这归因于内源鼠BAT中葡萄糖的摄取增加,而不是移植细胞对葡萄糖的摄取增加。内源性scWAT或骨骼肌中的葡萄糖摄取或任何上述基因的表达没有变化。从功能上讲,与接受白色对照细胞的小鼠相比,接受HUMBLE或棕色对照细胞的小鼠的内源性BAT附近的表面温度更高,提示受体小鼠适应性生热的激活。这些数据表明,HUMBLE和棕色对照细胞可以激活内源性BAT。
结果与讨论
在本研究中,研究人员使用CRISPR-SAM系统工程改造了人类白色前脂肪细胞,以激活内源性UCP1基因并驱动类似棕色的表型。通过利用配对的人类白色和棕色前脂肪细胞系能够将工程改造的HUMBLE细胞及其同基因的亲本白色对照细胞与同一个体的真正的棕色对照细胞进行比较,从而提供准确的表型比较。研究数据证明了CRISPR工程化的HUMBLE细胞在预防和治疗肥胖症方面的临床前治疗潜力。HUMBLE细胞的移植可大大改善小鼠体内的葡萄糖稳态。
在研究中,移植的人类前脂肪细胞原位分化为脂肪细胞,更重要的是在肥胖的小鼠模型中,脂肪细胞功能所需的血管化和神经支配得以发展。此外,移植的细胞在体内存活了至少12周,因此这些细胞对小鼠体内葡萄糖稳态的有益作用得以持续。结果表明,基于HUMBLE细胞的疗法可潜在地用于对抗高热量饮食引起的代谢紊乱。
此项研究存在一定的局限性,研究人员使用免疫功能低下的裸鼠作为HUMBLE细胞移植的受体,以避免人类细胞移植的免疫排斥。但是,免疫受损的小鼠中特异性免疫细胞和细胞因子的缺乏可能会影响代谢评估的结果和解释。CRISPR这一被称为“魔剪”的基因编辑工具在基因工程应用方面被寄予厚望,其凭借着成本低廉、操作方便以及效率高等优点已经成为了生物科研的得力助手,但不可否认的是CRISPR目前仍然面临着易脱靶等等的问题与挑战,美迪西作为新药研发CRO也会继续关注基因编辑技术的发展,期待CRISPR技术发展成熟的那一天,为人类健康贡献力量。
关于美迪西
美迪西(股票代码:688202)成立于2004年,总部位于上海,致力于为全球制药企业、研究机构及科研工作者提供全方位的临床前新药研究服务。美迪西的一站式综合服务以强有力的项目管理和更高效、高性价比的研发服务助力客户加速新药研发进程,服务涵盖医药临床前新药研究的全过程,包括药物发现、药学研究及临床前研究。美迪西与国内外优质客户共同成长,为全球超过700家客户提供新药研发服务,美迪西将继续立足全球视野,聚力中国创新,为人类健康贡献力量!
联系我们
Email:
marketing@medicilon.com.cn
电话: +86 (21) 5859-1500(总机)









