美迪西生物医药在仿制药质量一致性评价方面,已成功完成了多个质量一致性评价案例,具有仿制药研发丰富的经验,能够为您提供更专业的一致性评价服务。
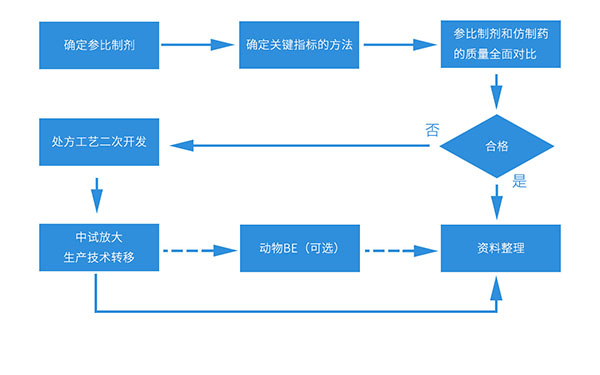
美迪西仿制药质量一致性评价综合服务平台可以提供以下综合服务:
一、参比制剂和仿制药的质量全面比对:
-
确定四条溶出曲线的测定条件,测定参比制剂和仿制制剂的溶出曲线,进行溶出曲线的比对;
-
确定有关物质、异构体等方法,测定参比制剂和仿制制剂的有关物质、含量、异构体等;
-
研究参比制剂和仿制制剂所用原料药的晶型;
-
稳定性研究(包括影响因素、加速和长期);
二、处方工艺二次开发服务:
-
需更深入地研究原研制剂的质量;
-
对原料药的性质进行充分的研究;
-
调整优化处方和工艺,并通过逐级放大确保处方工艺的耐用性;
-
中试放大/生产技术转移;
-
质量研究
三、动物BE服务
本公司具有符合GLP资质的动物实验室和检测中心,可以用比格犬或食蟹猴等大动物进行动物BE实验,为制剂的优化提供数据支持,降低临床BE风险。
美迪西仿制药质量一致性评价中心的优势
-
专业的工作背景,已成功向FDA和CFDA申报了多个仿制药品种;
-
完整的质量保证体系,保证数据的准确性、真实、可追溯和完整性;
-
高效的工作流程,规范的操作标准,完善的方案和报告模板;
-
先进的仪器设备,包括光纤在线检测自动溶出仪和符合GMP固体制剂中试车间等,保证项目完成的效率和时间;
-
拥有良好的临床研究合作伙伴;
资讯内容如下:
2月29日,国务院食品安全办公室主任、国家食品药品监督管理总局局长毕井泉在国务院新闻办举行的发布会上表示:在过去的一年里,食品药品监管部门认真落实习近平总书记“最严谨的标准、最严格的监管、最严厉的处罚、最严肃的问责”的要求,认真贯彻落实党中央、国务院工作要求和改革部署,以信息公开为突破口,增加食品药品检查、抽样检验的范围和频率,严厉查处食品药品领域的违法犯罪行为,在第一时间公开抽检结果、公开检查结果、公开案件查处结果,维护消费者权益,震慑违法犯罪,约束执法者的行为,发挥社会舆论的监督作用,促进了社会诚信体系建设。我们还积极推进药品审评审批制度改革。提高了药品的审批标准,按照与原研药品质量、疗效一致的原则对新申请上市的仿制药进行技术审评,对已经上市的仿制药开展一致性评价。简政放权,提高效率,推进药品上市许可持有人的试点,促进制药工业由生产大国向质量强国转变。
提高食品药品监管透明度
据介绍,当前我国正处在食品药品安全矛盾高发期,保障食品药品安全,任重道远。在新的一年里,食药监管部门将按照党中央、国务院的要求,继续加强市、县两级食品抽样检验和生产经营企业、餐饮企业的日常检查;整治农药兽药残留超标和添加剂滥用等违法行为;切实加强标准的制定、法规的完善、药品研发相关技术指导原则起草等基础性工作;继续加大对各类食品药品安全违法犯罪的打击力度;继续做好检查检验和案件查处信息公开工作;提高食品药品监管透明度,增强公众对中国制造食品药品的信心;加快完善统一权威的食品药品管理体制和制度,努力打造一支技术过硬、作风优良、勤政廉洁的职业化监管队伍。
在食品方面,新修订的《食品安全法》2015年10月1日起正式开始实行。目前,国家总局已经制定发布了和正在制定一些配套的规章,确保切实把法律规定的内容执行到位。
同时,将进一步加强如婴幼儿配方乳品等重点领域的监管,如对婴幼儿乳粉的抽验,从去年每个季度抽样检验公布一次改成“月月抽检、月月公开”,还要继续加大生产体系的检查力度,严格控制婴幼儿配方乳粉配方的数量和品牌,禁止利用配方进行夸大宣传、误导消费者。
此外,在加强对生产企业、销售企业日常监督的同时,鼓励企业按国务院文件要求建立产品追溯体系,确保产品的源头可追溯。
毕井泉说,企业是食品药品研发和生产的主体,应当承担起保障质量安全的主体责任,应当承担起建设产品追溯体系的主体责任。
据悉,此前热议的电子监管码问题也将得到妥善解决。在今后政策措施的制定时,充分考虑其经济性、有效性、公平性、合法性,充分听取社会各界的意见,取得监管对象的理解、配合和支持。
药品审评审批提质增效
据介绍,药品审评积压是国家总局目前面临的一个比较艰巨的任务,药品审评积压最高的时候曾经达到32000多件,经过一年多的努力,去年药品审评中心审评完成的数量比2014年增加了90%,药品审评积压的数量大幅度下降。
2月26日,国家总局发布《关于解决药品注册申请积压实行优先审评审批的意见(食药监药化管〔2016〕19号)》以进一步加强药品注册管理,加快具有临床价值的新药和临床急需仿制药的研发上市,解决药品注册申请积压的矛盾。
据悉,下一步将建立药品上市申请人与药品审评人员的会议交流制度,实施对罕见病及其他特殊病种等减少临床试验病例数,以及对治疗严重危及生命的疾病无有效治疗手段的新药允许在Ⅲ期临床前有条件的批准上市等一系列措施,鼓励新药加快上市。
此外,对于国内缺乏且临床急需的儿童用药,国家总局设立了申报审评的专门通道,加快审评。1月29日,国家总局专门发布了《关于临床急需儿童用药申请优先审评审批品种评定基本原则及首批优先审评审批品种的公告》,进一步细化了相关政策,鼓励企业研发上市适合儿童使用的药品以及研发儿童专用剂型和规格。
明确一致性评价时间节点
据介绍,2月20日,国务院办公厅正式印发《关于推进仿制药质量和疗效一致性评价的意见》(以下称《意见》),《意见》明确:企业是仿制药一致性评价的主体,应主动选购参比制剂开展相关研究,按规定的方法研究和进行临床试验,确保产品质量和疗效与参比制剂一致;政府要统筹协调产品参比制剂的确认、评价方法和资料申报、评价,以及对仿制药一致性评价工作加强指导。同时,对通过仿制药一致性评价工作的药品在临床使用和医疗保险方面给予政策上的支持。
同时,《意见》还明确要求:国家基本药物目录(2012年版)中2007年10月1日前批准的化学仿制药口服固体制剂,应在2018年底完成一致性评价,逾期未完成的不予再注册。对其他已批准上市的药品,自首家品种通过一致性评价后,其他生产企业的相同品种在3年内仍未通过评价的,注销药品批准文号。
毕井泉说,这对企业来说也是一个巨大的挑战,但是这项工作对提高制药工业的发展质量,对于真正把我国制药工业由制药大国转为制药强国,真正使我们所生产的制剂药品能够走向国际市场,都是至关重要的。
强大的监管才能造就强大的产业。食品药品企业既是食药监管部门的监管对象也是服务对象。各级食药监管部门要寓监管于服务之中,以有效的监管制度创新服务于产业的发展创新,推动食品药品产业的供给侧结构性改革,夯实食品药品安全的产业基础。食品药品是民生问题,也是社会问题,希望社会各界积极参与食品药品监管工作,推动食品安全社会共治,同各级食药监管部门一起努力,共同维护好广大人民群众“舌尖上的安全”。






 相关新闻
相关新闻