FDA新药获批率持续走高
还记得FDA上次驳回药品上市申请是什么时候吗?
在2008年,制药公司申请销售从未上市过的药物——即FDA所称的“新分子实体”,驳回率高达66%。然而,今年截至目前,FDA只拒绝了这些新分子实体申请的其中3个用法,通过了25个,获批率达89%。
这些数据来自于BioMedTracker,其是出版巨头Informa下属的一个部门,旨在帮助投资者对制药行业进行跟踪。进一步深入挖掘这些数据可以发现,驳回率的下降幅度更大。
BioMedTracker的统计口径与FDA略有不同。在其统计中,2015年的申请驳回数量包括了艾尔建(Allergan)的一款院内感染新抗菌药物Avycaz,以及礼来(Eli Lilly)和勃林格殷格翰(Boehringer Ingelheim)的二甲双胍组合——糖尿病药物Jardiance被驳回的申请。事实上,Avycaz已经被批准了另外两个适应症,而Jardiance也是已上市药物。
所以,FDA更确切的批准率应该是96%。除去BioMedTracker对同一种药物多用途的计数,FDA通过了23个药物的上市申请而只驳回了1个,即默沙东(Merck)的麻醉解药Bridion。
大开绿灯
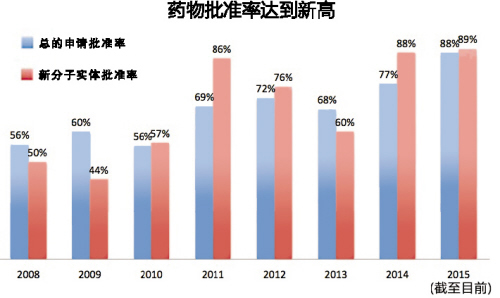
以BioMedTracker的统计数据为参考,比较过去7年间的药物获批率,从中可以看出,FDA对新药上市开绿灯变得越来越频繁。
BioMedTracker的数据显示,2008年FDA批准了20个新分子实体,拒绝了20个,获批率为50%。2009年,新分子实体获批率降到44%,28个被拒绝,22个被批准。2011年,获批率上升到86%,部分是由于之前被驳回的药物成功上市。而到2013年,获批率又下降到60%,去年则又再升到88%。从制药公司的角度来看,这些证据表明,其正处在药物获批上市的黄金时期。
还有更多的数据可以证明这一论点,BioMedTracker不仅追踪了这些新分子实体,还密切追踪制药公司向FDA提交的每一次申请。在其统计资料中,包括了制药公司向FDA提交的新药上市申请和已上市药物的新用途申请。
2008年,制药公司向FDA提出了134个申请,获批75个,获批率为56%。药物申请获批率在2009年和2010年保持稳定,然后分别在2011年、2012年和2013年上升到70%左右。去年,获批率更是飙升至77%,126个申请中有97个通过了批准。今年截至目前,获批率已高达88%。制药公司向FDA提出已上市药物的新用途申请,十有八九能获批。
或已触顶
FDA指出,药物获批率上升的一个原因是,这正是美国国会所期望的工作。FDA有一个批准新药上市的最后期限,而它正尽力在这之前完成工作。更重要的是,FDA制定了一个新的程序来确保制药公司在新药申请提出前就与其取得了良好的沟通。FDA还成立了一个项目来关切患者权益主张者的诉求,许多患者更希望FDA批准一个具有边际收益的药物。
现在来看,药物获批率上升的趋势还会持续。7月份得到美国众议院通过的《21世纪治愈法案》(21st Century Cures Act),试图进一步加快药物审批并去除一些繁琐的程序。
但审批提速的风险也显而易见。在1990年代末与2000年代初之间有个新药获批的繁荣期,1999年,FDA批准的两个药物成为了药品安全丑闻的代名词:Vioxx,最终由默沙东撤市;葛兰素史克(GlaxoSmithKline)的Avandia,则在后来的使用中受到严格限制。
药物获批数量的激增是好的,前提是其不会导致另一次关于药物安全的争论。当前的高批准率值得业界谨慎,FDA几乎都会批准药物上市,适当降低罕见病药的标准进行得如此之快,这是不是已经到顶了?
这似乎也给了生物技术投资者一个警告。虽然对于任何在短期内面临着FDA决定的药物来说,高批准率是一个好消息。而当前也正是前所未有的生物技术繁荣时期,iShares纳斯达克生物科技指数在过去5年上涨了360%,部分原因是制药公司的监管环境已有所改善。但如果有高达96%的新药可以通过批准,那意味着获批率只能下降,这可能是就是行业触顶的迹象。

分享到:






 相关新闻
相关新闻