CDE药品审评周报(2015.12.20-2015.12.26)
本周63个药品(按受理号计,下同)进入在审评阶段,53个药品进入审批阶段,而有298个药品审批完毕,260个药品制证完毕,请先看重点药物:
重点药物
1、PLB1003胶囊:本品的原料及2个规格的胶囊剂均由北京浦润奥生物科技有限责任公司申报,为1.1类化药,适应症为抗肿瘤,目前靶点还未知。2015年6月北京浦润奥获得1.1类新药伯瑞替尼肠溶胶囊的临床批件,目前未在审评中心临床试验登记中心查到关于伯瑞替尼的临床信息。PLB1003胶囊是该公司申报的第二个1.1类新药,目前已进入在审评状态。
2、注射用头孢妥仑磷酸钠:本品的原料及注射剂均由四川科伦(股票代码SZ002422)药物研究院有限公司申报,为1.1类化药。头孢妥仑4代头孢类药物,目前国内已进口上市头孢妥仑匹酯片,为头孢妥仑的羧酸酯,而科伦申报的为头孢妥仑的磷酸钠盐,给药途径也由口服变为注射。本品2014年4月承办,为特殊审批品种,经过1次发补,目前获批临床。不过受限抗令的影响,不知市场会怎样。
3、双醋瑞因片:本品由安士制药(中山)有限公司5类申报,目前待生产现场核查。双醋瑞因为骨关节炎IL-1的重要抑制剂,用于治疗退行性关节疾病(骨关节炎及相关疾病),目前国内仅有1家企业进口上市双醋瑞因胶囊,且双醋瑞因片也仅有安士制药1家申报,此外安士制药还进口申报了双醋瑞因的控释片,这个很看好这个品种吗?
4、注射用重组人胸腺素β4:本品由北京诺思兰德生物技术股份有限公司(股票代码SB430047)申报,为1类治疗用生物制品。本品2014年4月进入审评中心,属于重大专项品种,经历1次发补,历时20个月,目前审评完毕,获批临床。重组人胸腺素β4可应用于急性心肌梗死、皮肤损伤、角膜损伤和干眼症,市场前景广阔啊。
距《Oh My God,11月份又来1300多个临床批件》发布还不到一个月,临床批件数量又上涨了1000多,达到4357件;咸达在12月15日的文章《当撤回变成一种周更》中统计的撤回数量已经达到727个,这两周撤回数量又增加137个,也许CFDA又要发公告了。本周审批完毕的药物中,获批临床以及撤回的药品见下图:
获批临床化药新药
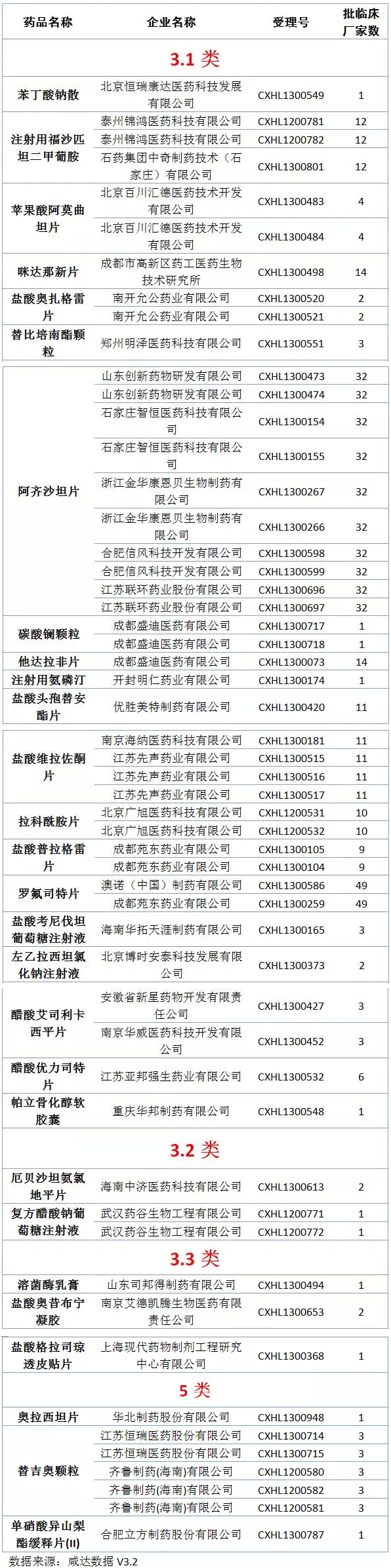
仿制药
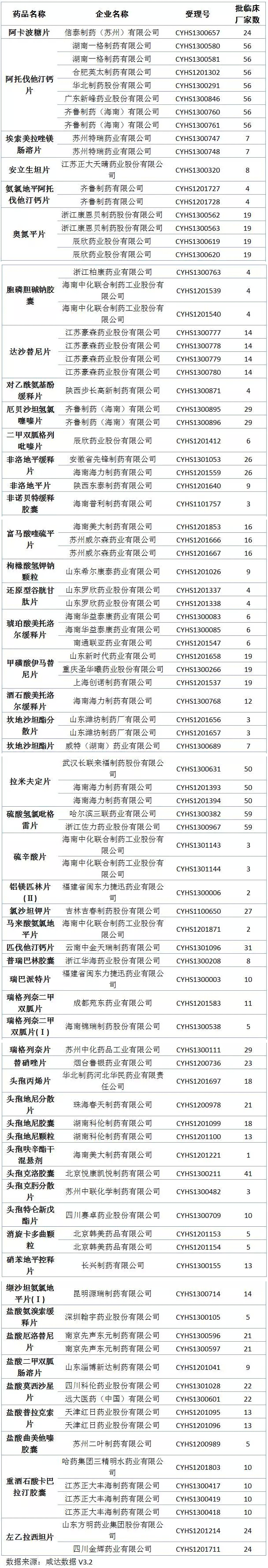
生物制品
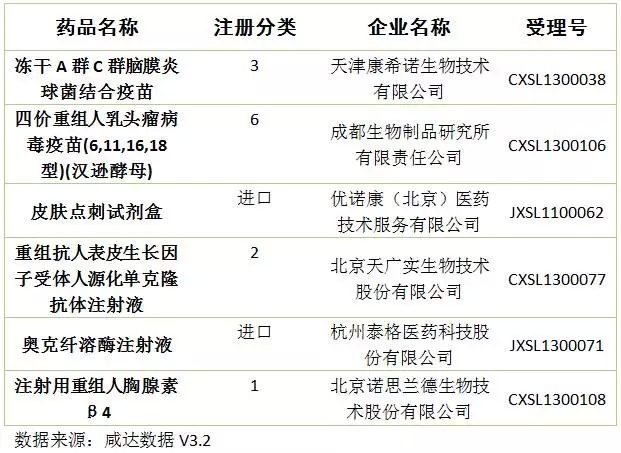
撤回申请化药新药
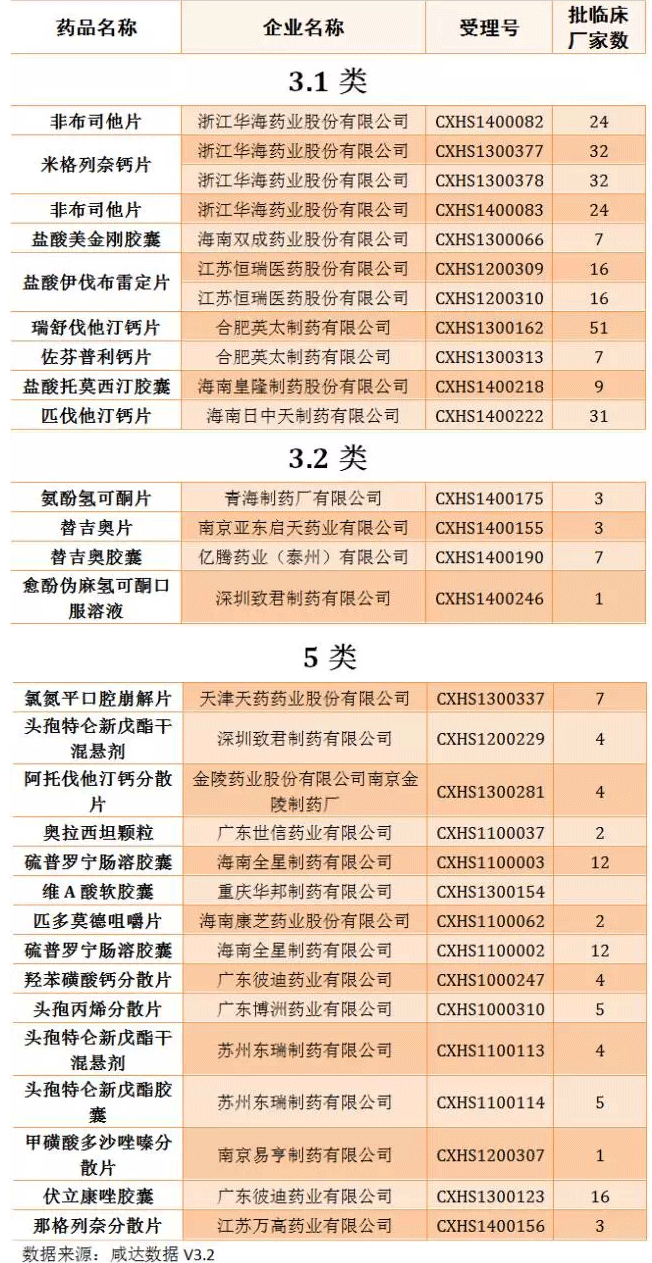
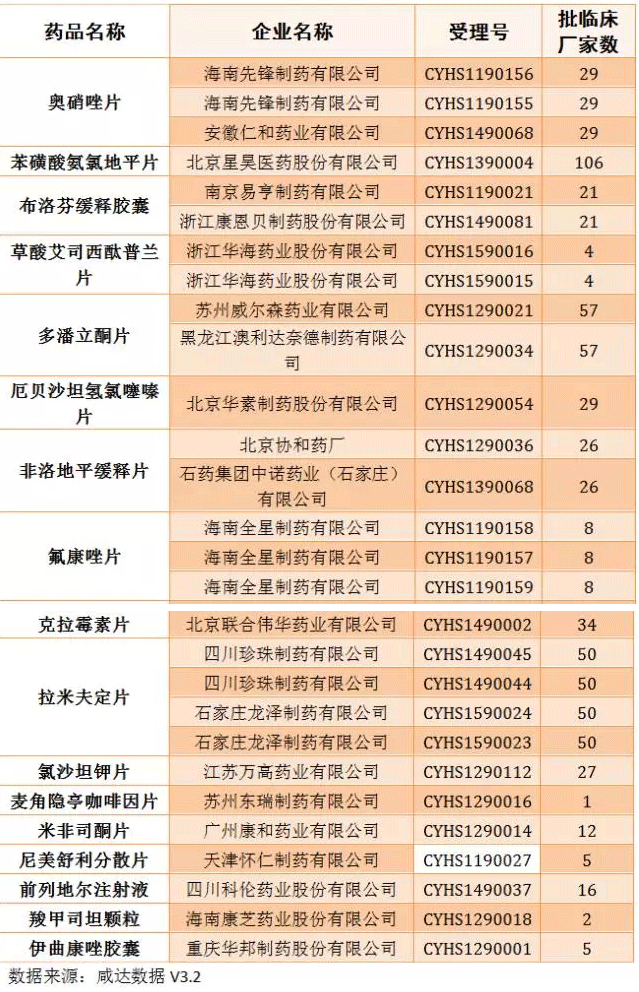
仿制药

分享到:









 相关新闻
相关新闻