专利药到期,仿制药增多让中国原料药市场迎来新机遇
Fiercepharma网站一份分析报告分析2015年专利到期原研药的累计价值高达440亿美元。在过去,由于中国产业化水平有限,那些拥有原辅料资源的优势并未在国际上体现,而现在中国产业化能力不断上升,因专利药的到期,一大波中国药企跟风仿制或者进行技术创新,间接拉动了原料药的需要,一旦传统的原料药企转型成功,其带来的价值将不可估量。
近年来,业内一直在呼吁关注全球仿制药浪潮带来的机遇,具体在国内,到底机会在哪里?根据IMS的统计,2015年是专利药到期的大潮,拉动了特色原料药的快速发展。
Fiercepharma网站一份分析报告分析2015年专利到期原研药的累计价值高达440亿美元。由于因专利药的到期,一大波仿制药企跟风仿制,这间接拉动了原料药的需要。
中国原料药之路,路宽且长
1)得上游原料制剂者得天下
众所周知,中国是世界上最大的番茄红素原料供应;世界上最大的葡萄籽原料供应;世界上最大的胶原蛋白原料供应;世界上最大的酵母原料供应;世界上最大的银杏原料供应;世界上最大的螺旋藻原料供应;中国医药工业组成化学药(包括化学原料药、制剂)占据45%的份额。中国生产化学原料药1500余种,产量达200万吨,年产量超万吨的品种有青霉素、阿莫西林、维生素C、维生素E等。以青霉素、维生素C为代表的20余种化学原料药生产和出口量均居世界第一;没有哪个国家的自然界物种有中国这么丰富,这也是为何中医能诞生在中国的原因。
2)中国原料药企的不足,亟需转型
由于我国医药产业的技术能力和生产管理水平以及对仿制药的认识程度较低以及对原辅料来源的选择、原料晶型控制、处方及工艺参数的筛选及试验稳定性等方面的研究不够;我国拥有原辅料资源的优势并未在国际上体现。屠呦呦女士对传统材料的提取分离而发现了青蒿素,让我们意识到了在拥有资源的背景下,不断提高技术获得成功的可能性指日可待。
笔者在与一位制药业前辈的聊天时,聊到原料药企的原型时,表示若是这些企业将传统的资源当做垫脚石,发力于现阶段有前景的生物制药,尤其是以CAR-T和PD-1为核心的免疫疗法时,其成功的概率更大。
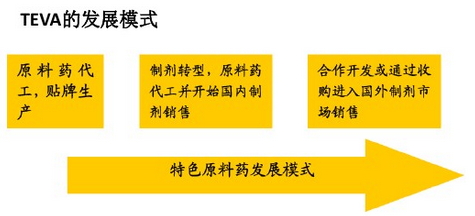
3)从TEVA的成功模式学习用仿制药带动原料药增长
以色列的梯瓦制药(TEVA)从一个原料药代工、贴牌生产的企业向制剂转型,再通过合作/收购进入了国际制剂市场,并跃居为全球制药企业top20。
2009年,原料药业务为梯瓦制药带来了5.65亿美元的销售收入。相比较138亿美元的销售总收入,梯瓦制药的原料药似乎显得无足轻重。不过,考虑到梯瓦制药原料药供应的“自给自足”以及它所带来的一体化的向前整合竞争优势,小小的原料药撬动了一个大杠杆,令整个梯瓦几乎可以无所不能地生产各种各样的药物,而且也为公司赢得首仿药提供重要保障。原料药生产优势由此演化为梯瓦制药的秘密武器。
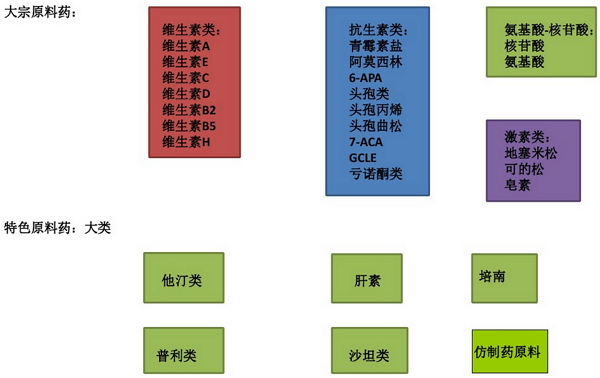
4)在资源大国生产可以节省大量的运输和进出口成本
中国生产化学药品制剂4000余种,基本能满足国家防治病的需要。中国医药企业目前共拥有药品批准文号18.7万个,其中化学药品批准文号为12.1万个,绝大部分为仿制药。他汀类、普利类、沙坦类特色原料药已成为新的出口优势产品。
随着多个“重磅”药物专利到期,中国仿制药产业正迎来2014年-2020年的七年时间里,将有2590亿美元的药品面临专利到期,尽管世界药品市场仅以年均4%-5%的低速增长,然而仿制药正以年均11%的增幅, 46%的市场份额或将会被仿制药所占有,世界仿制药规模已从2007年的890亿美元,增长到2014年的1800亿美元,2015年中国仿制药市场规模或将接近5000亿元。由于中国的原料药材丰富,也正迎来了一个前所未有的机遇期。2014年国际原料药市场总销售额高达1340亿美元,其中出口总金额160亿美元,进口总金额85亿美元。
5)人口老龄化加剧催生药品需求量
由于中国60岁以上的人口已超过2亿人,老龄化正在加速。研发一个全新的生物药至少需要10到20年的时间,在今后10-20年难以依靠自主创新药物满足临床一线需求,仿制药在今后仍将是中国医药卫生体系的支撑和基本保障,这更是催生了原料药市场的需求。毫无疑问,“小剂量、高效价”是今后原料药发展的方向。
不过原料药市场的发展离不开政府支持企业集中抢仿即将到期的专利药并出口到欧、美、日市场,并建立绿色通道,提高仿制药审批效率;促进仿制药质量一致性评价,提高仿制药质量。
美迪西“仿制药质量一致性评价”服务介绍
“仿制药质量一致性评价”主要针对2007年新版《药品注册管理办法》颁布实施之前批准的口服仿制药,主要包括片剂、胶囊剂和颗粒剂等,进行质量再评价。评价要求考察国内企业生产的产品与原研产品在溶出度和有关物质等关键质量指标上是否一致。如果质量不一致,则要求企业对产品进行处方工艺改进。
考虑到国内仿制药质量大多数达不到原研产品的水平,因此“质量一致性评价”的具体业务一般包括两个部分:
1.对企业产品的溶出度和有关物质与参比制剂进行对比,根据研究数据判断两者质量是否一致。
2.如果质量不一致,则需要按照仿制药研发的要求,对该产品的处方工艺进行重新开发,将开发好的新处方工艺移交给企业并且支持企业进行申报。
联系我们:marketing@medicilon.com.cn 电话:02158591500

分享到:






 相关新闻
相关新闻