
Emai:marketing@medicilon.com.cn
业务咨询专线:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦东新区川大路585号
邮编:201299
电话:+86 (21) 5859-1500(总机)
传真:+86 (21) 5859-6369
© 2023 上海美迪西生物医药股份有限公司 保留所有权利 沪ICP备10216606号-3


业务咨询
中国:
Email: marketing@medicilon.com.cn
业务咨询专线:400-780-8018
(仅限服务咨询,其他事宜请拨打川沙总部电话)
川沙总部电话: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




不久前,CFDA发布《中国上市药品目录集》,这是我国首次发布上市药品目录集,第一批被收录的药品有131个品种,203个品规。在众多品种中,注射用培美曲塞二钠因是唯一一个被提名且被收录的注射剂类化学仿制药而备受关注。瞬间“注射剂的评价”等相关信息刷爆朋友圈,中药注射剂受影响再次成为“老生常谈”的话题。
一直以来,中药注射剂的疗效、安全性等问题屡被诟病,“封杀”“停用”等字眼常见诸报端,使得中药注射剂长期处于风口浪尖。2009年发布的《关于做好中药注射剂安全性再评价工作的通知》称,将分期分批对中药注射剂的重点品种进行风险效益评价,第一批拟开展风险效益评价的品种为双黄连注射剂和参麦注射剂。随后公布的第二批再评价品种包括鱼腥草注射液和鱼金注射液。
去年2月,2017版医保目录正式发布,包含中药注射剂49个。其中,39个受到不同程度限制,占比高达80%。在受限品种里,有26个限二级以上医疗机构使用,也就是说基层医院不能使用。新增的中药注射剂只有3个,且均为独家品种(益母草注射液、舒肝宁注射液和瓜蒌皮注射液)。随后,CFDA宣布“要启动中药注射剂药品安全性、有效性的再评价工作”,正式传递了中药注射剂再评价将成为下一阶段的攻艰任务,并将此作为推进整体药品质量疗效工作重点之一的信号。
2017年7月1日,我国首部中医药法《中华人民共和国中医药法》正式实施,提出建立符合中医药特点的管理制度,加大对中医药事业的扶持力度,坚持扶持与规范并重,加强对中医药的监管,同时加大对中医药违法行为的处罚力度,中药注射剂的评价工作再次迎来关键环节。10月,《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(简称《意见》)发布。《意见》提出将严格药品注射剂审评审批,中药注射剂的评价工作将大刀阔斧进行。
CFDA相关负责人曾公开表示,“中药注射剂不仅要评价安全性,还要评价有效性。有效性是药品的根本属性,如果没有效这个药品就没有价值,所以中药注射剂的评价首先是评价有效性,同时也要审查安全性”。
中药注射剂一直是不良反应的重灾区,也一直是相关部门监测的重点。2016年,25万例的中药不良反应/事件报告中,注射剂和口服制剂所占比例分别为53.7%和38.6%。报告特别指出,中药注射剂占比较高,需要继续关注其安全用药风险。
公开资料显示,2006年因安全问题,鱼腥草注射液被暂停使用和审批;2008年茵栀黄注射液和刺五加注射液引起不良反应,分别造成3例和1例患者死亡;2009年发生双黄连注射液致死事件,相关部门因此撤销了人参茎叶总皂苷注射液和炎毒清注射液2个品种的药品标准;2017年9月,CFDA紧急召回2款中药注射剂:红花注射剂和喜炎平注射剂,因为它们引起了部分患者寒战、发热等不良反应,红花注射剂已被检测出热源不稳定,喜炎平注射剂导致不良反应的原因还有待进一步检测。此次事件又把中药注射剂推向了风口浪尖。
目前,引起中药注射剂的不安全性因素主要包括:
(1)源头问题:中药材和制药辅料的品质控制难。除了药材本身,生产过程中使用的辅料如添加剂、助溶剂、稳定剂、稀释剂等也可能与中药成分发生反应或交联而形成致敏原。但是目前对于很多生产过程中的辅料,并没有明确规定剂量,这也是一个危险因素。
(2)生产工艺和稳定性不可控。中药注射剂生产环节复杂,涉及药材种植、炮制、提取、中间体、成品等多个步骤,这些过程都可能带入树脂、重金属、蛋白质、鞣质等有害物质;生产过程中因灭菌、灌封等工艺不合格,导致热源等的产生,引发不良反应。
(3)有效成分或组分的毒副作用。成分或组分只能在一定剂量范围内发挥作用,超过剂量就可引发毒副作用。
(4)临床数据不充分,药品说明不够详尽。
截至2017年12月31日,CFDA批准上市中药注射剂979个,涉及生产企业两百多家,品种138个(CFDA搜索“国产药品”“中药”“注射”关键词出现979条)。
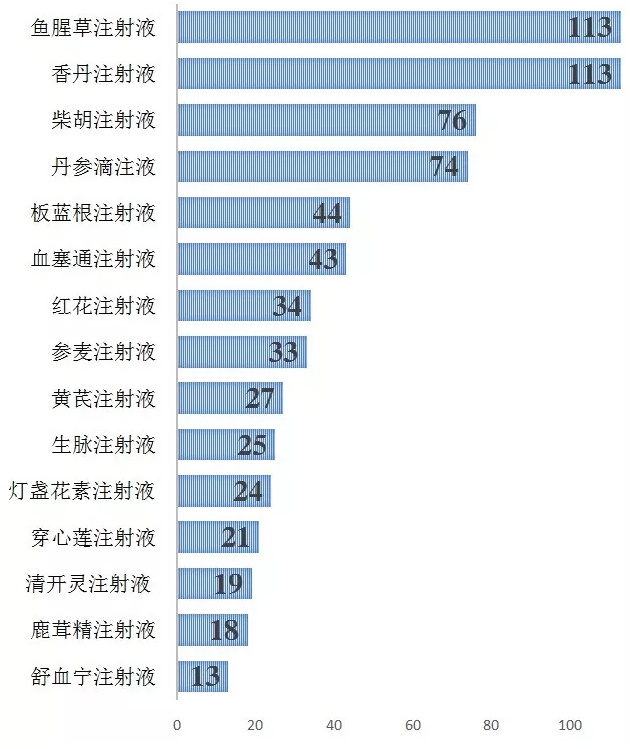
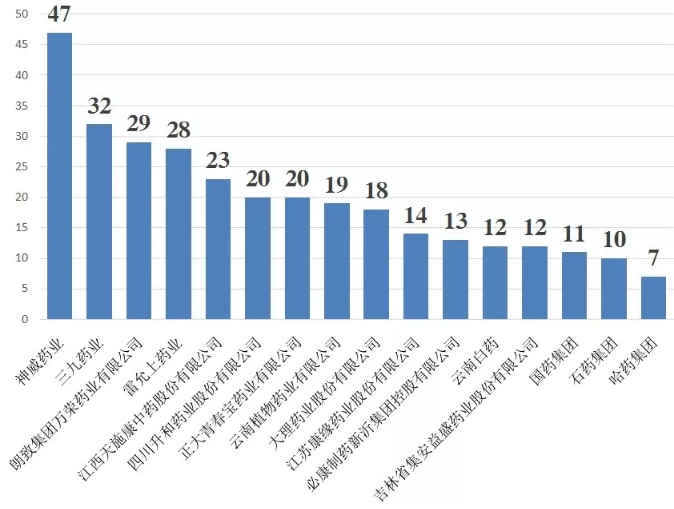
其中,中药注射剂批文数量最多的品种为鱼腥草注射液和香丹注射液,分别有113个产品获批生产。而神威药业、三九药业和万荣药业分别以47个、32个和29个批文占据中药注射剂批文数量TOP15企业前三甲。
 相关新闻
相关新闻