背景
从2015年开始,国内医药政策发生了颠覆性的改革,这股风暴一直刮到了2017年。国家药监局、卫计委陆续出台了一系列政策法规,从内容上主要可以分为三类:医改政策、药品审评审批政策和仿制药一致性评价。影响的几大主体包括:国内药企、外资药企、医院、CRO、CSO和患者。对抗癌新药创新这一块,支持的力度更是前所未有,包括优先审评、简化审批程序、快速进入医保等政策的推行将加速创新药在我国的上市速度,让创新药尽快的惠及更多的患者。
忆往昔峥嵘岁月,模式不再可复制
在以上新政实施前,因为中国特殊的药品审批政策所致,进口新药在中国的上市往往比国外要晚3-8年,国内的患者因为无法及时使用这些新药,而错过了最佳治疗的机会,尤其是抗肿瘤药物,“用的早,用的好”是能最好发挥药物疗效的关键因素,例如,在多西他赛用于非小细胞肺癌的使用上,一线使用的有效率几乎是二线使用的一倍;由于抗肿瘤新药开发投资巨大,近些年又在不断上升,所以定价比较昂贵,这是一个限制新药可及性的关键因素,医保更新速度太慢(间隔至少5年),在日本,新药上市几个月就可以进入医保;在国内,新药进入医保的难度很大,进口药更是难以实现。很多患者根本用不起这样的高价药。
在这里,不得不提到一个很成功的案例,埃克替尼,是首个由我国医药企业开发的拥有自主知识产权的小分子络氨酸激酶抑制剂,上市以后很快打开市场并取得成功(历年的销售额见图1)。上市第二年就达到3.07亿元的销售额,2016年埃克替尼的销售额高达10.35亿元。
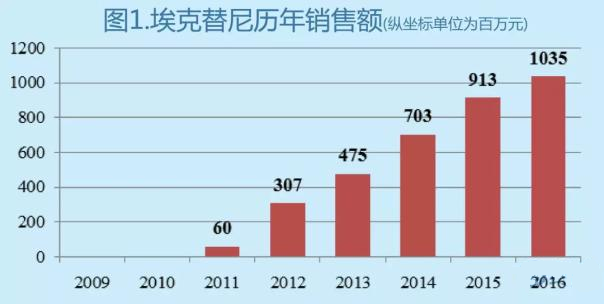
埃克替尼取得的成功,可能有以下几个原因:
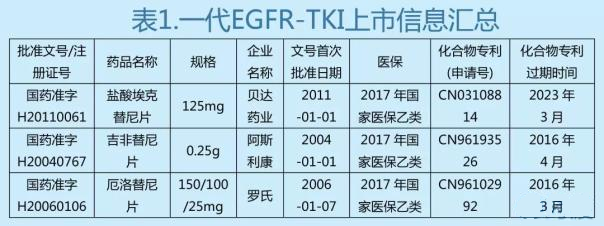
①埃克替尼上市这几年,吉非替尼和厄洛替尼的专利还尚未到期,三家企业均未受仿制药竞争带来的影响。
②从2011至2016年,国内上市的非小细胞肺癌的EGFR-TKI药物仅有一代药物吉非替尼和厄洛替尼,二代药物阿法替尼在2017年4月获得批准上市,三代药物奥希替尼在2017年3月被批准上市。没有面临二、三代药物的竞争,而且,短时间内阿法替尼、奥希替尼还无法影响整个用药格局。
③公司市场销售能力强,又具有本土作战带来的主场优势,在2013年被部分省纳入医保目录,享受国家优惠待遇。
④埃克替尼经过多个大型RCT试验验证,包括与吉非替尼的头对头研究ICOGEN,证明其疗效和安全性不劣于吉非替尼,缺点是需要一日服用三次,依从性不及吉非替尼。又被《中国晚期原发性肺癌诊治专家共识(2016年版)》等指南推荐。
从以上的分析我们也可以看到,好品种+好销售+合适的上市时机三合一因素铸就了埃克替尼的成功。但成功已经不能复制,2017年以后EGFR-TKI的竞争将更加复杂,由于研究表明二代和三代EGFR-TKI均可以用于EGFR敏感突变的NSCLC患者的一线治疗,而且还可以用于一代EGFR-TKI无法治疗的其他突变,再加上仿制药陆续开始上市,未来EGFR-TKI之间的竞争将会十分惨烈,但一代EGFR-TKI具有疗效好、价格低、医保报销、医生使用经验丰富四大法宝,还不会很快失去一线治疗的地位。
忽如一夜春风来,千树万树梨花开
早在2015年11月11日,国家局就发布了“国家食品药品监督管理总局关于药品注册审评审批若干政策的公告(2015年第230号)”,是近几年第一次针对新药审批做出较大的改革,共包括10项政策,其中3条政策(第3、7、8条)对创新药的审批和市场准入、未来的市场发展均有很大的影响。包括:对新药的临床试验申请,实行一次性批准,不再采取分期申报、分期审评审批的方式;加快临床急需药品的审批,实行单独排队,艾滋病、恶性肿瘤、重大传染病和罕见病药品均被列为急需药品。
而2017年10月10日,《国家食品药品监督管理总局关于调整进口药品注册管理有关事项的决定》(国家食品药品监督管理总局令第35号)被公示在总局网站上,以往进口药品在中国进行临床试验和上市注册申请需要在国外批准上市才可以;在中国进行国际多中心药物临床试验,试验用药物需要满足已在境外注册,或者已进入Ⅱ期或Ⅲ期临床试验的要求(预防用生物制品除外);进口药注册需要三报三批;这些因素均导致了进口药物在我国上市要晚于发达国家3-8年。所以,与发达国家相比,我国的用药结构一直是很落后的。此次调整取消了上述规定,并提出:对在中国进行的国际多中心临床试验,允许同步开展Ⅰ期临床试验;在中国进行的国际多中心药物临床试验完成后,申请人可以直接提出药品上市注册申请;而且同样适用于该决定发布前已受理、以国际多中心临床试验数据提出免做进口药品临床试验的注册申请,只要这些申请符合《药品注册管理办法》及相关文件要求的,可以直接批准进口。以上这些政策将加快国外创新药物进入国内的速度,同时,加剧国内外创新型企业的竞争。
关于优先审评这一块,早在2015年11月13日,总局就已经发布了《关于解决药品注册申请积压实行优先审评审批的意见(征求意见稿)》,2016年2月26日正式发布《解决药品注册申请积压实行优先审评审批的意见》,2017年12月28日,总局发布《关于鼓励药品创新实行优先审评审批的意见》,同时废止了2016年2月26日正式发布的《解决药品注册申请积压实行优先审评审批的意见》。从内容上看,新旧法规给出优先审评的范围基本没变,新的意见仅增加了将实施强制许可的药品纳入优先审评审批的范围。标题上从“解决积压”变成“鼓励创新”,加快具有临床价值、临床优势、临床急需的药品上市速度仍是不变的主题。
受以上政策惠及的包括阿法替尼、奥希替尼等进口创新药,2017年4月,阿法替尼在中国被批准上市,提出注册申请后,在2016年10月10日被CDE公示获得优先审评资格,理由是“本品为首个第二代EGFR-TKI,与目前国内已上市的第一代EGFR-TKIs相比,具有明显的临床优势”。阿法替尼是首个“上市申请”获得优先审评的进口新药。虽然在阿法替尼的用药过程中,多数患者需要通过剂量调整来克服(相对于一代EGFR-TKI)本身存在毒性较大的缺点,但其对于EGFR罕见突变的患者很有效。奥希替尼片(AZD9291)在2016年8月提出国内注册申请,2016年11月3日被CDE公示获得优先审评资格,2017年3月24日被国家食药总局批准上市,成为我国新药审批改革后上市审批时间最短的药物,也是阿斯利康管线中批准最快的药物。
小结
从以上的内容我们看到,国家在新药创新的支持方面,还是做了大量的工作,尤其是一些有价值的抗癌新药实现了在短期内批准上市,未来将会有更多有价值的创新药会驶入CFDA铺建的快车道。在看到机遇存在时,同时对我国的药企、CRO、CSO也提出了更高的要求,药企需要提高项目管理能力和研发创新能力,CRO需提高自己的临床试验业务水平,CSO需提高自己的销售业务水平。
参考文献:
1.药渡数据库
2.CFDA官网
3.CDE官网
4.中国埃克替尼治疗非小细胞肺癌专家共识(2016年版)









 相关新闻
相关新闻