癌症免疫疗法就是通过重新启动并维持肿瘤-免疫循环,恢复机体正常的抗肿瘤免疫反应,从而控制与清除肿瘤的一种治疗方法,包括单克隆抗体类免疫检查点抑制剂、治疗性抗体、癌症疫苗、细胞治疗和小分子抑制剂等。近几年,癌症免疫疗法的好消息不断,目前已在多种肿瘤如黑色素瘤,非小细胞肺癌、肾癌和前列腺癌等实体瘤的治疗中展示出了强大的抗肿瘤活性。癌症免疫疗法由于其卓越的疗效和创新性,在2013年被《科学》杂志评为年度最重要的科学突破。
不过,癌症免疫疗法仅对部分患者有效果。近年来,科学家们先后发现很多因素影响癌症免疫治疗效果,比如肠道细菌的组成;树突细胞的抗原呈递能力;T细胞的增殖能力;特定的免疫细胞类型,如骨髓衍生性抑制细胞、调节性T细胞(Treg)、天然T细胞和CD14+CD16-HLA-DRHi免疫细胞;染色质重塑复合物缺乏;HLA基因型;等等。基于此,小编针对这方面近年来取得的进展,进行一番梳理,以飨读者。
1、利用模拟抗原呈递细胞的生物材料支架促进T细胞高效增殖
doi:doi:10.1038/nbt.4047
免疫学家和肿瘤学家正在利用过继细胞转移技术,操纵人体的免疫系统来抵抗癌症和其他疾病。在正常的免疫反应中,一种被称作T细胞的白细胞经另一种被称作抗原呈递细胞(APC)的免疫细胞的指导后扩大它们的数量,并且保持存活。过继细胞转移程序正是在培养皿中模拟这一过程,即从患者身上取出T细胞,让它们繁殖,有时对它们进行基因修饰,然后将它们移植回患者体内,这样它们就能够找到并杀死癌细胞。然而,这些程序通常需要数周的时间才能产生大批量的治疗性T细胞,其中这些T细胞的数量是非常庞大的,而且它们的活性要足以消除它们的靶细胞。
如今,在一项新的研究中,由美国哈佛大学怀斯生物启发工程研究所和约翰-保尔森工程与应用科学学院的David Mooney教授领导的一个研究团队报道了一种基于替代材料的T细胞扩增方法,这可能帮助克服这些障碍。利用一种模拟APC的生物材料支架,这些研究人员实现了比现有方法更好地促进小鼠和人类原代T细胞增殖;并且他们在经过表达嵌合抗原受体的T细胞(CAR-T细胞)治疗的小鼠淋巴瘤模型中证实了这种方法的潜力,其中这些CAR-T细胞经过基因改造后靶向破坏淋巴瘤细胞。相关研究结果于2018年1月15日在线发表在Nature Biotechnology期刊上,论文标题为“Scaffolds that mimic antigen-presenting cells enable ex vivo expansion of primary T cells”。
T细胞三维透视图,图片来自CC BY 3.0, Blausen.com staff。
为了设计一种模拟APC的支架,这些研究人员首先将白细胞介素2(IL-2)---一种由APC产生的因子,能够延长相关的T细胞存活---装载在微小的介孔硅棒(mesoporous silica rods, MSR)中。他们随后利用形成薄薄的类似于APC的外膜的支撑性脂质双层(SLB)的脂质包被MSR,接着利用一对激活T细胞的抗体对这种支撑性脂质双层进行功能化处理,这样这些抗体在脂质层中移动并且能够结合T细胞表面上的受体/辅助受体分子。在培养基中,三维支架通过MSR沉降和随机堆积而自发形成,并且产生足够大的孔从而允许T细胞进入、移动和聚集,从而提供让它们增殖的信号。
在进行一系列的并行比较中,Mooney团队证实模拟APC的支架的性能优于商业上可获得的增殖珠(Dynabeads),这些增殖珠当前用于临床过继细胞转移方法中。论文第二作者、Mooney 实验室研究生David Zhang 说,“在单剂量注射中,APC模拟支架导致小鼠和人类的原代T细胞增殖增加了2~10倍。另一个优势是,APC模拟支架能够让我们调整在想要的免疫反应中发挥不同作用的T细胞亚群的比例,在未来这可能会增加它们的功能。”
2.抗原呈递细胞中的PD-L1表达或可预测哪些患者受益于癌症免疫治疗
doi:10.1172/JCI96113
在一项新的研究中,Zou和同事们针对这个问题提供一个重要的线索。相关研究结果于2018年1月16月在线发表在Journal of Clinical Investigation期刊上,论文标题为“Host expression of PD-L1 determines efficacy of PD-L1 pathway blockade–mediated tumor regression”。
这些研究人员研究了患有结肠癌、卵巢癌、黑色素瘤和肺癌的小鼠,以便理解蛋白PD-L1的表达如何影响对PD-L1阻断作出的反应。这是免疫治疗药物的关键靶标。他们发现了抗原呈递细胞---在肿瘤微环境和附近的淋巴结中发现的巨噬细胞和树突细胞---中的一个关键环节。
在这项新的研究中,这些研究人员研究了来自接受免疫疗法治疗的黑色素瘤和卵巢癌患者的组织样本。在这两种癌症中,他们发现表达PD-L1的抗原呈递细胞所占的比例与对治疗作出的客观临床反应之间存在着关联。
3.促进癌症治疗的新型免疫疗法
doi:10.1038/nmeth.4579
最近,来自EPFL的研究者们构建出了一种新的分子,该分子能够帮助免疫系统识别以及杀伤肿瘤细胞。相关结果发表在最近一期的《Nature Methods》杂志上。
来自EPFL的研究者们设计出了人工的受体分子EVIR(extracellular vesicle-internalizing receptors),这一设计能够确保树突状细胞选择性地捕获符合患者体内实际情况的抗原分子。首先通过吧EVIR嵌入到树突状细胞中,让其识别'外泌体'中的蛋白质。
通过成像的手段,作者发现EVIR能够促进肿瘤抗原从外泌体表面向树突状细胞膜上转运。基于上述结果,作者认为这一发现为设计更为高效的肿瘤免疫疗法提供了新的方向。
4.新型免疫疗法增强人体杀死癌细胞的能力
doi:10.1016/j.cell.2017.12.026
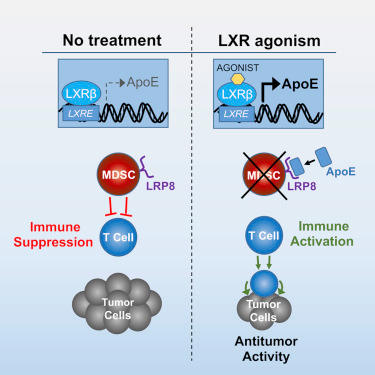
如今,在一项新的研究中,来自美国洛克菲勒大学的研究人员报道了一个避开癌症的保护性屏障而使得免疫细胞更容易完成它们的工作的方法。这种方法着重关注被称作骨髓衍生性抑制细胞(myeloid-derived suppressor cell, MDSC)的免疫细胞,并且似乎能够破坏小鼠中的多种不同的癌症类型。再者,来自这种治疗方法的首个临床试验的结果揭示出它有效地激活杀死癌细胞的免疫细胞。相关研究结果于2018年1月11日在线发表在Cell期刊上,论文标题为“LXR/ApoE Activation Restricts Innate Immune Suppression in Cancer”。
图片来自Cell, doi:10.1016/j.cell.2017.12.026。
当这些研究人员发现了激活ApoE表达的药物在那些具有健康免疫系统的小鼠中比在那些没有健康免疫系统的小鼠中能够更加有效时,事情就开始变得更加有趣了。除了抗肿瘤转移作用之外,这些药物似乎通过降低这些小鼠中的MDSC水平来影响免疫反应,并因此激活抗肿瘤的T细胞,随后这些T细胞能够破坏癌症。论文第一作者、Sohail Tavazoie实验室访问科学家Masoud Tavazoie说,“这些发现提示着激活ApoE通路可能增强抵抗癌症的免疫反应。”
在当前的这项新的研究中,这些研究人员给予患有不同类型癌症的小鼠一种被称作RGX-104的化合物,其中已知这种化合物诱导身体产生ApoE。经证实这种化合物高效地抵抗多种肿瘤类型,特别是肺癌、肾癌、卵巢癌和乳腺癌,以及黑色素瘤和胶质母细胞瘤。它杀死了这些小鼠中的MDSC,而且他们证实杀死这些细胞允许其他的免疫细胞进入和摧毁癌症。
5、特定肠道共生细菌能够提高癌症免疫疗法的治疗成功率
doi:10.1126/science.aao3290; doi:10.1126/science.aar2946
基于抗PD-1抗体的免疫疗法已经对癌症治疗产生重大影响,但是仅让一部分患者受益。导致不同患者之间出现不同治疗反应的一个原因可能是患者的不同的微生物组组成。在临床前小鼠模型中已经证实,微生物组组成影响抗肿瘤免疫反应和免疫治疗的疗效。Vyara Matson等人通过将针对选定细菌的16S核糖体RNA基因测序、宏基因组鸟枪法测序和定量聚合酶链式反应整合在一起,分析了来自接受免疫疗法之前的转移性黑素瘤患者的基准粪便样品。这些作者们观察到共生微生物组成与临床反应之间存在着显著的关联性。在对免疫疗法作出反应的转移性黑素瘤患者中更为丰富的细菌物种包括长双歧杆菌(Bifidobacterium longum)、产气柯林斯菌(Collinsella aerofaciens)和屎肠球菌(Enterococcus faecium)。将来自对免疫疗法作出反应的转移性黑素瘤患者的粪便材料移植到无菌小鼠中能够更好地控制肿瘤、增强T细胞功能和实现更大的抗PD-L1抗体药物的疗效。这些的研究结果提示着共生微生物组(commensal microbiome)可能对人类癌症患者的抗肿瘤免疫反应产生着重要的影响。
6.肠道细菌影响免疫疗法抵抗上皮性肿瘤的效果
doi:10.1126/science.aan3706; doi:10.1126/science.aar2946
在一项新的研究中,来自法国的一个研究团队分析了249名接受了抗PD-1免疫治疗的肺癌、肾癌等多种上皮性肿瘤的患者,其中有69名患者在免疫治疗开始之前或刚开始时,接受了抗生素治疗 。他们发现这些接受抗生素治疗的患者对这种免疫治疗药物产生原发耐药性,很快就出现癌症复发,而且具有更短的存活期。这就说明抗生素治疗极大地影响免疫治疗的效果:抗生素抑制这种免疫治疗药物给晚期癌症患者带来的临床益处,而且这种原发性耐药是由于异常的肠道微生物组组成导致的。相关研究结果于2017年11月2日在线发表在Science期刊上,论文标题为“Gut microbiome influences efficacy of PD-1–based immunotherapy against epithelial tumors”。
为了寻找其中的因果机制,这些研究人员对这种免疫疗法作出反应的癌症患者和未作出反应的癌症患者的肠道微生物组进行比较。他们发现一种被称作Akkermansia muciniphila的有益细菌的 相对丰度与癌症患者对这种免疫疗法作出的临床反应相关联。在此之前,人们已发现这种细菌具有预防肥胖和糖尿病的作用。在这项新的研究中,他们发现它能够增强这种免疫疗法的效果。 随后,这些研究人员将来自对这种免疫疗法作出反应的癌症患者和未作出反应的癌症患者的粪便微生物组移植到无菌的或者接受抗生素治疗的小鼠体内,发现那些接受来自对这种免疫疗法作 出反应的癌症患者的粪便微生物组移植的小鼠对这种免疫疗法作出的反应得到更好的改善。此外,那些接受未作出反应的癌症患者的粪便微生物组移植的小鼠口服这种有益细菌补充剂后也能 够通过将CCR9+CXCR3+CD4+ T细胞招募到肿瘤床中,以一种依赖于IL-12的方式恢复对这种免疫疗法作出的反应。这些结果再次表明肠道微生物组调节着癌症免疫疗法的效果。
7.肠道细菌调节黑色素瘤对免疫疗法作出的反应
doi:10.1126/science.aan4236; doi:10.1126/science.aar2946
在一项新的研究中,来自美国德州大学MD安德森癌症中心的研究人员报道生活在人肠道中的细菌能够如何影响癌症对免疫疗法作出的反应,这为改进治疗的研究开辟新的途径。相关研究结果 于2017年11月2日在线发表在Science期刊上,论文标题为“Gut microbiome modulates response to anti–PD-1 immunotherapy in melanoma patients”。 通过分析转移性黑色素瘤患者的 粪便样品来评估这些患者的肠道微生物组,这些研究人员发现如果这些患者含有更加多样化的肠道细菌群体或者大量的某些细菌,那么他们接受抗PD1免疫检查点阻断治疗后能够在更长的时间 内控制他们的疾病。
免疫检查点阻断药物会激活人体自身的免疫系统来攻击癌细胞,从而让大约25%的转移性黑色素瘤患者受益,但是这些免疫治疗反应并不总是持久的。为了评估肠道微生物组的影响,Wargo和 同事们分析了接受抗PD1免疫治疗的患者的粪便样品和口腔拭子(buccal swab),其中口腔拭子是来自脸颊内的组织样品,而抗PD1免疫治疗阻断T细胞表面上的对免疫系统起着抑制作用的PD1 蛋白。他们开展16S rRNA测序和全基因组测序来确定口腔拭子和粪便微生物组的多样性、组成和功能潜力。
结果表明对抗PD1免疫治疗作出反应的患者(肠道中具有较高的有益的梭菌/瘤胃球菌水平)具有更多的T细胞进入到肿瘤中和更高水平的杀死异常细胞的循环T细胞。那些具有更高拟 杆菌水平的患者具有更高水平的循环调节性T细胞、髓源抑制性细胞(myeloid derived suppressor cells)和减弱的细胞因子反应,从而抑制抗肿瘤免疫反应。
最后,这些研究人员通过粪便微生物组移植(fecal microbiome transplant, FMT)将来自对抗PD1免疫治疗作出反应的患者和不作出反应的患者的粪便微生物组移植到无菌的小鼠中。那些接 受来自作出反应的患者的粪便微生物组移植的小鼠具有显著下降的肿瘤生长和更高水平的有益T细胞和更低水平的免疫抑制性细胞。当接受免疫检查点阻断治疗时,它们也具有更好的治疗结果 。
8.揭示出黑色素瘤抵抗免疫治疗之谜
doi:10.1126/science.aao1710
癌症科学家面临的一个紧迫的问题就是为什么免疫疗法在一些患者中取得了显著的效果,但对大多数患者是没有效果的。如今,来自美国达纳-法伯癌症研究所的两个研究小组独立地发现了癌细胞中的一种影响着它们是否对被称作免疫检查点抑制剂的免疫治疗药物产生抵抗力或作出反应的遗传机制。这些发现揭示出潜在的新型药物靶标,并且有可能将免疫治疗的益处延伸到更多的患者和更多的癌症类型。相关研究结果于2018年1月4日在线发表在Science期刊上,论文标题为“A major chromatin regulator determines resistance of tumor cells to T cell–mediated killing”。
图片来自Yueyao Zhu and Wei Guo。
这个研究小组都发现了对免疫检查点抑制剂的抵抗作用受到一组调节着DNA在细胞中如何包装的蛋白发生的变化的严格控制。这组被称作染色质重塑复合物的蛋白是SWI/SNF;它的组分是不同的基因编码着的,其中包括ARID2、PBRM1和BRD7。SWI/SNF的作用是打开紧密缠绕的DNA片段,这就使得它的蓝图能够被细胞读取,从而激活某些基因表达。他们鉴定出SWI/SNF染色质重塑复合物的PBAF亚型参与抵抗免疫T细胞的杀伤作用。
当PBRM1基因在实验中被敲除时,这些黑色素瘤细胞对T细胞产生的干扰素-γ变得更加敏感,并且作为应答,产生招募更多的抵抗肿瘤的T细胞进入肿瘤中的信号分子。据这些研究人员所称,PBAF复合物中的另外两个基因ARID2和BRD7也在一些癌症中发生突变,而且这些癌症,如缺乏ARID2功能的黑色素瘤,可能也对免疫检查点抑制剂作出更好的反应。
9.揭示转移性肾癌抵抗免疫检查点抑制剂治疗机制
doi:10.1126/science.aan5951
对于癌症科学家来说,一个迫切的问题就是为什么免疫疗法在一些患者中取得了显著的效果,但对大多数患者是没有效果的。如今,来自美国达纳-法伯癌症研究所的一个研究小组发现了癌细胞中的一种影响着它们是否对被称作免疫检查点抑制剂的免疫治疗药物产生抵抗力或作出反应的遗传机制。这些发现揭示出潜在的新型药物靶标,并且有可能将免疫治疗的益处延伸到更多的患者和更多的癌症类型。相关研究结果于2018年1月4日在线发表在Science期刊上,论文标题为“Genomic correlates of response to immune checkpoint therapies in clear cell renal cell carcinoma”。
由Van Allen和Choueiri领导的一个研究小组寻求解释为何一些患有转移性肾透明细胞癌(clear cell renal cell cancer, ccRCC)的患者从阻断PD-1检查点的免疫检查点抑制剂治疗中获得临床益处,有时甚至是持久的临床益处,而其他的患者则不会如此。
为了寻找ccRCC肿瘤中的影响免疫治疗反应或抵抗性的其他特征,这些研究人员利用全外显子组DNA测序技术分析了在一项临床试验中接受免疫检查点抑制剂纳武单抗(nivolumab)治疗的35名ccRCC患者的肿瘤样品。他们也分析了另一组63名接受类似药物治疗的转移性ccRCC患者的样品。
当对测序数据进行分类和细化时,这些研究人员发现受益于这种免疫治疗药物且具有更长的无进展生存期的患者是那些缺乏功能性PRBM1基因的患者。(大约41%的ccRCC患者具有非功能性的PRBM1基因)。这个基因编码蛋白BAF 180,该蛋白是染色质重塑复合物SWI/SNF的PBAF亚型的一个亚基。PBRM1基因功能丧失导致ccRCC癌细胞增加表达其他的基因,包括参与免疫系统激活的基因通路IL6/JAK-STAT3。
10.患者HLA基因型影响免疫检测点抑制剂的疗效
doi:10.1126/science.aao4572
被称作免疫检测点抑制剂(immune checkpoint inhibitor)的新药能够恢复对癌细胞的识别,从而导致对许多癌症类型产生显著的反应。但不是每名患者都会产生反应。在一项新的研究中,来自美国哥伦比亚大学赫伯特-欧文综合癌症中心和纪念斯隆-凯特琳癌症中心等研究机构的研究人员一直试图理解其中的原因,最终发现患者自身的基因如何能够在对免疫治疗药物作出的反应中发挥着作用。相关研究结果于2017年12月7日在线发表在Science期刊上,论文标题“Patient HLA class I genotype influences cancer response to checkpoint blockade immunotherapy”。论文通信作者为纪念斯隆-凯特琳癌症中心的Naiyer Rizvi博士和哥伦比亚大学赫伯特-欧文综合癌症中心的Timothy Chan博士。
图片来自National Institutes of Health。
涉及的基因属于人白细胞抗原(HLA)系统,即一种编码着免疫系统用来识别哪些细胞属于自身哪些细胞不属于自身的蛋白的基因复合体。HLA基因具有很多可能的变异,从而允许每个人的免疫系统对各种各样的外来入侵者作出反应。HLA系统将病毒或肿瘤的片段带到细胞的表面上,从而使得该细胞能够被免疫系统破坏。
这项新的研究探究了1535名接受免疫检查点抑制剂治疗的癌症患者,并发现具有更多的HLA基因版本(即具有更大的HLA基因多样性)对这种治疗更好地作出反应。
这项研究也证实具有较低的HLA多样性和较少的肿瘤突变的癌症患者并不那么好地对免疫检查点抑制剂作出反应。Rizvi博士和Chan博士之前一起证实细胞遭受损伤的程度和类型与对这些药物作出的反应存在着关联(Science, 03 Apr 2015, doi:10.1126/science.aaa1348),而这项新的研究则将患者的HLA与肿瘤遗传密码关联在一起。
11.罕见免疫细胞影响癌症免疫治疗效果
doi:10.1126/sciimmunol.aan4631
天然T细胞在癌症发生过程中的功能并不清楚,部分原因是由于效应T细胞能够直接调控肿瘤免疫反应的进程,因此研究者们将更多的精力放在后者上面,此外,天然T细胞在肿瘤微环境中的比例很少。
在最近这项发表在《science Immunology》杂志上的一篇文章中,作者等人发现肿瘤的代谢过程会影响天然T细胞的活性。肿瘤细胞往往需要大量的葡萄糖,而葡萄糖的代谢会产生乳糖。乳糖对于天然T细胞的功能具有负面的租用。一旦乳糖水平过高,T细胞将会受到严重的损伤,甚至导致死亡。
目前,预测癌症免疫治疗效果的研究重点都在记忆T细胞以及效应T细胞上,而这一新型的研究在提供了另外的可能。
12.特定免疫细胞活性能够限制免疫疗法的效果
doi:10.1038/ni.3868
最近,研究者们发现了一类关键免疫细胞的特殊功能,或许能够解释癌症免疫疗法的局限性。
Treg细胞是免疫系统中起着抑制免疫反应活性的作用。在正常情况下,T细胞能够抵抗外界侵染,而在任务完成之后,Treg细胞则会释放信号终止免疫反应。癌症的免疫治疗是通过提高免疫系统的活性来抵抗癌症,而Treg抑制免疫细胞的活性则能够限制癌症免疫疗法的效果。然而,临床试验表明单纯地清除体内的Treg细胞并没有增强癌症免疫疗法的效果,而其中的原因而并不清楚。
根据最近发表在《Nature Immunology》杂志上的一篇文章,作者认为清除Treg细胞并不等于阻止了它们所有的抑制活性。当Treg细胞死亡的时候,它们不仅不会失效,而且会变得更加有抑制能力,因此细胞死亡后整个免疫抑制的机器仍在运转。
而最近这项研究则表明,当Treg细胞死亡之后,他们仍会释放出大量的小分子代谢产物 ATP,常规情况下ATP能够帮助机体供能,而死亡后的Treg细胞则会快速地将ATP转化为腺嘌呤,腺嘌呤进一步靶向T细胞表明的一类受体,进而影响T细胞的正常功能。
13、肿瘤免疫治疗有没有效?看看这个标记物就知道!
doi:10.1038/nm.4466
目前,免疫治疗可以有效治疗黑素瘤和肺癌,这种方法主要通过使用机体正常情况下用于检测病原体和有害物质的免疫系统的功能达到肿瘤靶向治疗的目的。研究人员可以用特殊的抑制剂激活免疫细胞,使它们找出肿瘤细胞并清除它们。这种方式可以使原本很弱的免疫反应爆发,甚至可以检测和清除转移性癌细胞。免疫治疗可以控制50%的病人的肿瘤进展,甚至可以治愈癌症。 但是有一半的病人不但对免疫治疗无反应,还要遭受免疫治疗带来的副作用。来自苏黎世大学和苏黎世大学医院的一组研究人员使用了新方法以找出哪些病人可能对免疫治疗产生阳性反应。研究人员现在可以找出血液中预测免疫治疗是否有效的生物标记物。
分析细胞之后,研究人员与瑞士生物信息研究所的研究人员一起分析了数据,以找出可以预测治疗效果的分子模式。“令人惊讶的是,我们在免疫治疗之前就观察到血液中存在微弱的抗癌免疫反应,我们发现这个分子模式是CD14+CD16-HLA-DRHi免疫细胞,”Burkhard Becher说道。为了方便鉴定,生物标记物应该容易检测,而事实上传统的方法就可以在数秒内分析超过30个人的血液样品。







 相关新闻
相关新闻