国内首个“格列净”药物即将上市兼评国内注册分析
目前全球共有6款“列净”类单方药物上市,分别为:Canagliflozin(卡格列净/坎格列净)、Dapagliflozin(达格列浄)、Empagliflozin(恩格列净/艾格列净)、Ipragliflozin(伊格列净/依格列净)、Luseogliflozin(鲁格列净)以及tofogliflozin(托格列净)。其中FDA批准的只有前3种,后三种由日本厚生劳动省批准上市。卡格列净是FDA批准的第一款“列净”类药物(2013年3月获批),达格列浄是EMA批准的第一款“列净”类药物(2012年11月获批)。
目前国内有2款列净类药物已申报进口上市,分别为阿斯利阿康的达格列浄,以及勃林格殷格翰的恩格列净。
达格列浄:受理号为JXHS1500112和JXHS1500113,2015年12月承办,目前已于2016年6月16日灭灯,应该是已经审评完毕,审评时的备注为“食药监药化管便函[2014]729号过渡期品种”。达格列浄可能是国内上市的第一款“列净类”降糖药,市场可想而知。
恩格列净:受理号为JXHS1600050和JXHS1600051,2016年5月承办,目前还未进入序列,根据达格列浄的速度,可能半年后会审评完毕。
目前FDA批准的第一款卡格列净还未在国内申报上市,近期又出现卡格列净可能导致下肢截肢(主要是脚趾)风险增加而受到FDA和EMA关注的消息,不知其安全性是否会延伸至本类药物的安全性。
下面说说国内1.1类列净以及3.1类列净的申报情况吧:
首先,1.1类和3.1类没有上市申请,均为临床申请,从去年集中审评开始已陆陆续续有很多企业获得临床批件。
小编使用“列净”为药品的关键词在咸达数据V3.2数据库的注册库中进行模糊检索(截止时间2016年6月19日),共得到227个受理号,其中进口申请32个,新药申请192个(14个1.1类,170个3.1类,8个3.2类),补充申请3个。进口在此不多做介绍,主要介绍国内的申报:
首先呈现1.1类:
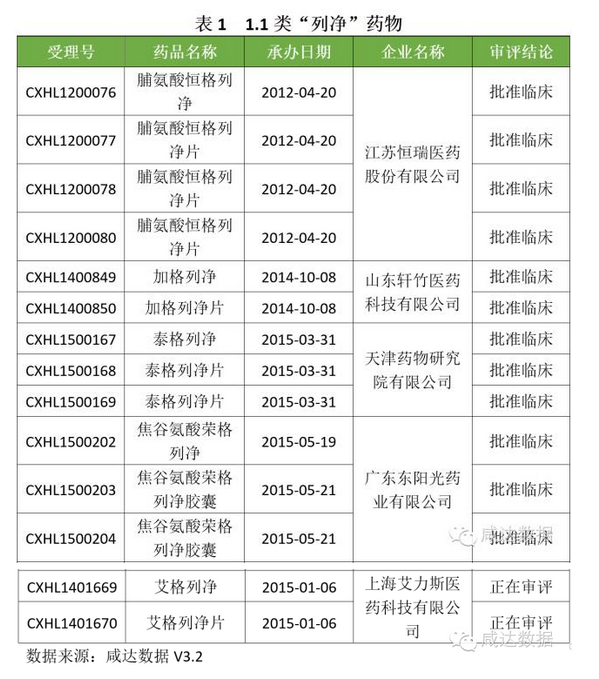
对于170个3.1类受理号,最多的是卡格列净及其片,共63个;其次是恩格列净及其片剂,共47个;再次是达格列浄及其片剂,共38个;第四是依格列净及其片剂,共17个;最后是托格列净,共2个受理号。
卡格列净:对于卡格列净目前已有18家公司审评完毕,其中江苏豪森、正大天晴、四川科伦、扬子江药业、天津市汉康、山东罗欣、齐鲁制药、湖北华世通、江苏先声、杭州华东医药、重庆医药工业研究院、南京卡文迪许等前后获得临床批件。豪森于今年年初第一个获得临床批件,目前还未在CDE临床试验公示平台上登记。此外,还有5家在CDE排队待审评。
恩格列净:对于恩格列净目前共有9家公司审评完毕,江苏豪森、山东罗欣、四川科伦、江苏奥赛康、正大天晴等分别前后获批临床。豪森又是第一家,于今年3月份获批,但是其余几家的获批时间相差不大,以后的临床之路还长着呢。同样,也没有临床试验的登记信息。此外,还有7家在CDE排队待审评。
达格列浄:对于达格列浄,目前共有9家审结完毕,江苏豪森、安徽联创、北京阳光诺和、石家庄智恒、湖北华世通、南京恩泰、南京卡文迪许等分别前后获批临床。江苏豪森再一次拔得头筹,在这里要热烈祝贺一下。同样,也没有国内企业的临床试验登记信息。此外,还有4家在CDE排队待审评。
依格列净:本品目前只有南京华威1家于今年5月份获得临床批件,其他有5家企业排队待审评。
托格列净:本品目前只有南京华威1家于今年申报,6月初底由CDE承办。
以上信息可以了解到,豪森应该是最大的赢家,正大天晴、南京华威、四川科伦、齐鲁制药等其他厂家也不是很逊色。至于谁能第一个仿制上市,那真的要看临床的真本事了。
对于8个3.2类药物,主要是卡格列净+二甲双胍以及恩格列净+利格列汀的申报,前者为哈尔滨珍宝和杭州华东医药2家申报,后者为山东罗欣1家申报。目前哈尔滨珍宝的已经处于审批阶段,而其他的仍然在审评。

分享到:








 相关新闻
相关新闻