
Emai:marketing@medicilon.com.cn
业务咨询专线:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦东新区川大路585号
邮编:201299
电话:+86 (21) 5859-1500(总机)
传真:+86 (21) 5859-6369
© 2023 上海美迪西生物医药股份有限公司 保留所有权利 沪ICP备10216606号-3


业务咨询
中国:
Email: marketing@medicilon.com.cn
业务咨询专线:400-780-8018
(仅限服务咨询,其他事宜请拨打川沙总部电话)
川沙总部电话: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




心脏安全性评价是各类新药进入临床试验前必须考察的一个重要的因素,也是创新药早期临床研究中最重要,难度较高的环节之一。近几年,一些已投入临床应用的药物因为其潜在的心脏毒性而受到药物安全管理部门和药物公司的广泛关注。美迪西作为一站式医药研发综合外包服务CRO公司,拥有经验丰富的专家团队,可提供从细胞到整体动物的多水平临床前心脏安全性评价服务。
开展心脏毒性试验,高效预测药物在早期心脏安全药理学方面的成药可靠性,对降低临床研究的潜在不良反应尤为重要,目前国内能提供符合GLP标准,且可用于IND申报包含心脏安全性评价的一站式医药研发服务公司为数不多,美迪西作为其中一员,服务详情如下:
体外安全性药理学研究
阐明化合物的非作用靶点不良反应(ADR)及作用靶点反应不均一所引起的不良反应,将有助于化合物通过后续的体内实验而避免潜在不良反应。
◆ 对先导化合物进行作用机理研究;
◆ 检测化合物对hERG离子通道的影响,提供其在药物筛选和开发等各阶段中对心脏安全性的综合性评价;
◆ 细胞水平的检测。
体内安全性药理学研究
◆ 无创遥测系统观察整体动物的心电图和血流动力学变化,可连续监测药物对心血管系统的影响。
临床前心脏安全性评价部分仪器

▲图1:Patch Clamp(膜片钳)
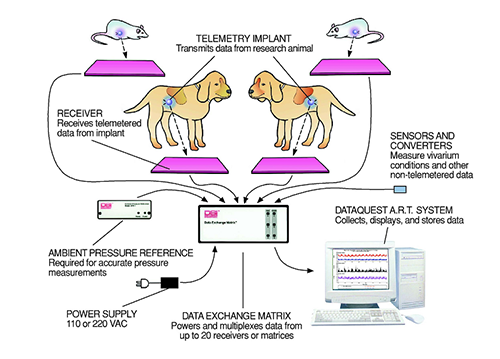
▲图2-1:DSI全植入式遥测系统
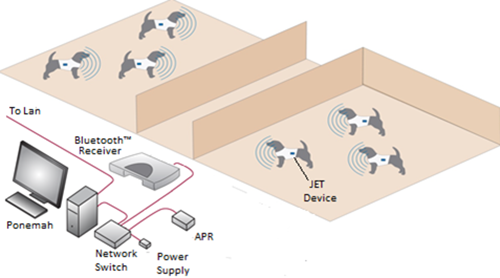
▲图2-2:DSI JET马甲式遥测系统
美迪西临床前心脏安全性评价优势
◆ 高性价比,研究周期短,项目启动快;
◆ 专家团队拥有非常丰富的项目经验,可提供建设性解决方案;
◆ 作为一站式医药研发外包服务公司,早期提供心脏毒性评价信息,有助于美迪西通过化学,药效、药代和制剂等一整套技术手段筛选出心脏安全系数更高的候选化合物。