一致性评价攻坚阶段,集中申报凸显
最近看到了很多关于新药融资、注册申报临床的新闻,今天笔者就来梳理一下仿制药的注册申报情况,尤其是在目前一致性评价所剩时间不多的情况下,仿制药做完生物等效性试验(BE)后在9月份CDE启动申请受理。预计最近一年仿制药一致性评价补充申请会出现集中爆发。按照政策要求,进行仿制药一致性评价的品种在启动BE之前应完成临床试验信息平台的登记,但是很多企业未登记公示,导致无法了解同品种的开展情况。
一致性评价对于医药行业的整体提升是件利国利民的好政策,一般研发实施关键环节包括“参比制剂备案(选择国家目录)— 处方工艺二次开发(药学研究)— BE备案 — BE试验 — 现场考核(省局)— 药检所复核 — 一致性评价申报 — CFDA审批”。目前来看,完成一致性评价工作整个流程大约需要20~28个月。
2016年一直纠结参比制剂,2017年一直在抢进度,殊不知很多品种已经过度备案,如苯磺酸氨氯地平片(11家)、阿莫西林胶囊(8家)、头孢呋辛酯(6家),这三个品种目前已经有注册申报。
目前的趋势是大药企,尤其是国内Top50的企业在一致性评价方面处于领先地位,主要是拥有足够的人、财、物去推动。虽然各地也推出了相关政策来鼓励进行一致性评价,如江西省、安徽省、哈尔滨市等最高一次性奖励通过的企业100万元、300万元和300万元。
图1 一致性评价申报受理品种一览
CDE的一致性评价受理品种按照接收号/受理号赋予原则:未改变生产线处方工艺的赋予CYHBXX(年份,两位)XXXXX国(4字头,五位大流水)的接收号;改变生产线处方工艺的一致性评价赋予CYHBXX(年份,两位)XXXXX国(5字头,五位大流水)的受理号。CYHBXX(年份,两位)XXXXX国(0字头)应该是9月份之前申报中检院一致性评价办公室。
此外,据笔者了解,国内销售额Top50 的固体制剂竞争也是相当激烈,阿托伐他汀钙片(北京嘉林、湖南迪诺、兴安药业)、瑞舒伐他汀钙片(京新、海正、天晴)、苯磺酸氨氯地平片、硫酸氢氯吡格雷片、富马酸替诺福韦二吡呋酯片等品种都已经有诸多厂家已经完成或者正在进行BE试验。
目前,受一致性评价政策利好的企业有:复星医药、石药集团、正大天晴、齐鲁、恒瑞医药、信立泰、扬子江、科伦摇曳以及做国际化的华海摇曳以及东阳光等。
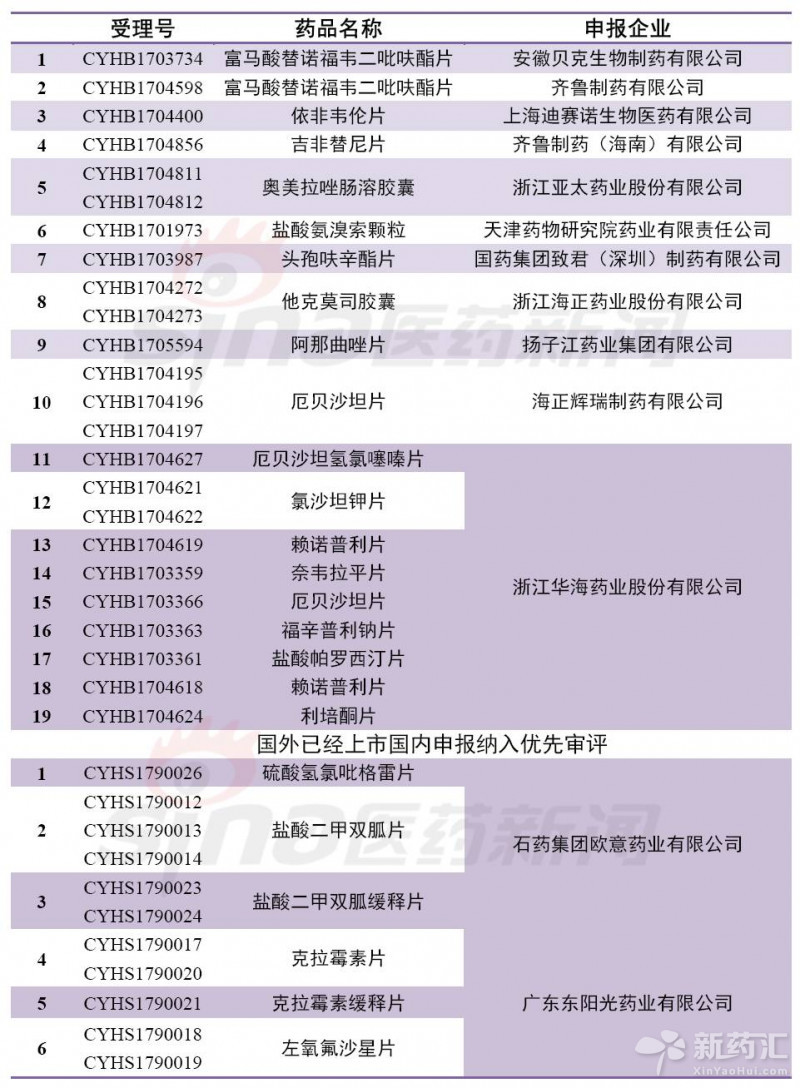
图2 其他一致性评价申报受理以及国外获批国内优先审评品种
总之,一致性评价对于中小型企业来说是生死攸关的时候,对于产品的选择至关重要,身为行业BD需要实时关注国内企业,从中寻找各种合作、投资机会。
以上数据来源于公开数据,仅统计了固体制剂的情况,不包括新化药4类的注册申报。如有疑问,欢迎留言补充。

分享到:








 相关新闻
相关新闻