2015新获批药物市场预期层级划分
审评积压一直是CFDA最为困扰的问题之一。根据公开数据,2014年最高峰时积压的审评数超过3万件。低水平重复申报无疑是导致审评数众多的首要因素。
药品批件是制药企业的核心竞争力之一,企业普遍热衷于增加手中的药品批件数量。比如上市药企,任何获得临床批件或生产批件的信息都会及时披露。而中国目前有6000家以上药厂和药品研发机构,如果每家每年仅申报1件,CFDA也将接收到6000件以上的申请。而根据CDE的2014年度(审评积压数量峰值年份)审评报告,包括埃索美拉唑和阿托伐他汀在内的8个化药品种,2014年新增申报厂家数都超过了100。
对于申报扎堆,CFDA也在寻找解决办法。从2015年下半年起,CFDA大幅加强了临床试验稽查,大量临床申报受理被撤回或被驳回。另一方面,加大了信息公开力度,引导企业理性开展新药研发。2016年初,官方及时发布了2015年申报审批信息,信息公开后可让各申报方对申报状况更为清楚,减少重复投入。同时,数据公开也能减少暗箱操作,保证信息透明。
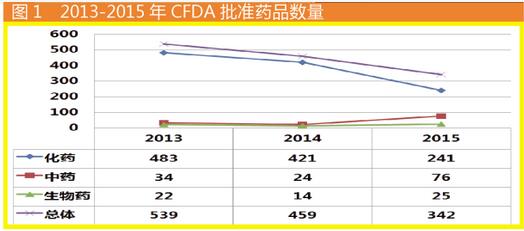
2015年批准药品总览
根据2015年CFDA统计数据,全年审批的药品共342种,从2013年起申报数量已持续第三年下降。不过,从细分类别来看,前些年一直受压制的中药似乎扬眉吐气,获批药品数增加了3倍;此外,生物药获批数量也有所增长。
获批药品数降低逾百种无疑来源于化药的“贡献”,2015年获批的化药数降低了180种。化药获批数量骤降与下半年大量品种退审密切相关。
中药获批数量虽大幅增加,但不少品种都是多个厂家的同一品种获批。大量的仿制中药集中获批无疑受益于2015年的集中审评制度。2016年初公布的国家级中医药规划,对中药行业而言无疑是振奋人心的,但中药的研发瓶颈依然制约着中药的发展,1类新药乃至5类、6类新药依然难觅。
相对于中药和化药,生物药依然扮演着小而精的角色——获批数量不多,但不乏精品。
新获批的342个品种,排除原料药和非治疗药物、合并同一厂家同一品种的不同规格后,剩余203个获批品种,包括75个中药、111个化药和17个生物药。
中药:批文数大增,扎堆申报需重视
75个新获批中药包括26个品种,大部分品种都是多家申报品种。比如地榆升白胶囊,来源于10个生产厂家;骨松宝片/丸,来源于8个厂家;调经祛斑片/丸,来源于8个厂家;乳癖舒片更是来源于13个厂家。
相对于仿制药和简单改剂药,中药新药的获批难度较大。不过,2015年中药新药获批数量大增,共有6个品种获批,分别是长白山制药的蒺藜皂苷胶囊、苏中的丹鹿胶囊、山东中大千方的槐芩软膏、河北医科大学制药厂的姜黄通络胶囊、北京中惠的五味苦参肠溶胶囊,以及鲁南厚普的首荟通便胶囊,其中蒺藜皂苷胶囊作为5类新药值得期待。

化药:国内品种缺亮点,关注进口重磅品种
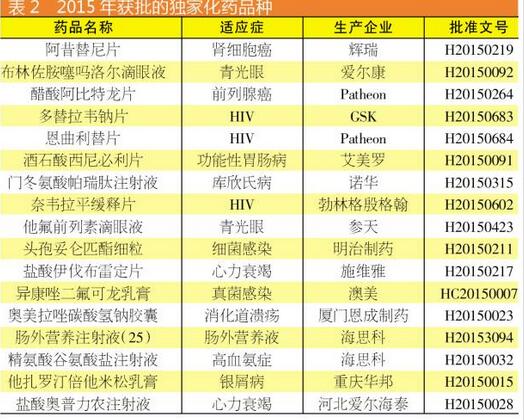
111个化药品种中,有12个为跨国企业首次进入中国的独家品种。其中,辉瑞的阿昔替尼、Patheon的阿比特龙、施维雅的伊伐布雷定等品种已经在国外取得了优秀的业绩,中国市场同样值得期待。
除了原研药,剩余的品种绝大多数都是仿制药。不过与中药不同,似乎集中审评并未与化药“结缘”,仅有氟哌噻吨美利曲辛、盐酸法舒地尔、帕洛诺司琼和注射用克林霉素磷酸酯这4个药物各有3个厂家产品获批,其余大多数仿制药仅有1~2个厂家获批。
国内申报的品种中,也有一些国内新上市的品种,包括厦门恩成的奥美拉唑碳酸氢钠、海思科的肠外营养注射液(25)和精氨酸谷氨酸注射液、河北爱尔海泰的奥普力农注射液。此外,华邦的他扎罗汀倍他米松乳膏是2015年唯一一个获批的国内一类新药。
生物药:6个首入市品种,疫苗自主研发出彩
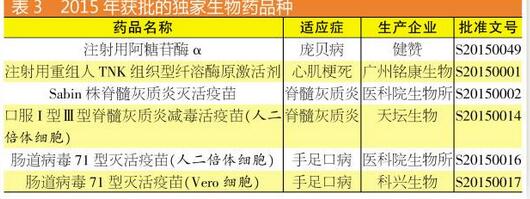
17个生物药中,既包括白蛋白、流感疫苗、狂犬病疫苗等多家企业生产的药物,也包括6个首次进入中国的品种。赛诺菲旗下健赞的注射用阿糖苷酶α的获批为国内庞贝病患者带来福音;广州铭康生物的注射用重组人TNK组织型纤溶酶原激活剂作为生物7类新药首次在中国获批,该药是急性心梗的特效药。
相比于治疗性生物药,2015年中国疫苗领域自主研发更为出彩,多个全新药品获批,主要针对脊髓灰质炎和手足口病。其中,医科院生物所的Sabin株脊髓灰质炎灭活疫苗是国内首个自主研发的灭活脊髓灰质炎疫苗,也是全球首个Sabin株的脊髓灰质炎灭活疫苗。此外,两个针对手足口病肠道病毒71型的灭活疫苗也开发成功,其中医科院生物所用人二倍体细胞培养的肠道病毒71型灭活疫苗非常值得期待。

分享到:







 相关新闻
相关新闻