CDE药品审评周报(2016.2.22-2016.2.27)
本周4个1.1类以及40个3.1类化药进入在审评阶段,3.1类中23个都是正大天晴的!此外,本周增加4个新的1.1化药审结完毕获批临床。
重点化药
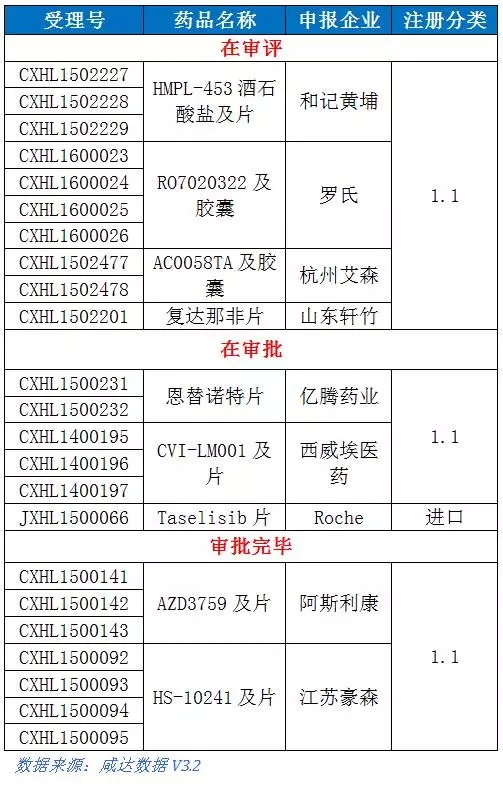
重点化药如下表:
重点生物制品
重点生物制品:本周3个1类治疗用生物制品进入在审评阶段:华博生物医药的重组人血管内皮生长因子受体-抗体融合蛋白眼用注射液、上海复宏汉霖的重组抗EGFR人源化单克隆抗体注射液、重庆智翔金泰的重组全人源抗EGFR单克隆抗体注射液。本周1个进口治疗用生物制品在国内首次获批临床:辉瑞的RN316注射液。
本周情况
以下小编具体介绍一下本周情况:
1、本周90个药品(以受理号计,下同)进入在审评阶段,其中40个3.1类,而正大天晴获取23个,包括艾德拉尼及片、琥珀酸曲格列汀及片、帕博西尼及胶囊、沙库比曲缬沙坦及片以及盐酸达卡他韦及片,等等。
2、本周202个药品进入在审批阶段,其中131个3.1类、6个6类,170个获得临床批件;424个药品审批完毕,其中243个获批临床,125个公告撤回;此外,仅13个药品制证完毕。
3、HMPL-453酒石酸盐及片:本品是一种新型的高选择性小分子成纤维细胞生长因子受体(FGFR)抑制剂,主要适应症包括小细胞肺癌,乳腺癌,多发性骨髓瘤,胃癌及膀胱癌。
4、RO7020322及胶囊:本品是罗氏申报的一款用于治疗慢性乙型肝炎的药物,目前在美国处于I期临床阶段。
5、AC0058TA及胶囊:本品推测与AC0058是一个东西,为全新机制小分子化合物,通过特异性抑制B淋巴细胞和其它炎症细胞的关键调节分子布鲁顿酪氨酸激酶(BTK),用于治疗系统性红斑狼疮和类风湿性关节炎等自身免疫性疾病。目前在美国已获得临床批件,将在美国开展I期临床研究。而在国内刚刚进入审评中心。
6、复达那非片:复达那非是具有全新特征的PDE-5抑制剂,为轩竹医药自主研发的第一个泌尿生殖系统药物,临床用于治疗良性前列腺增生症的症状与体征(BPH-LUTS)和勃起功能障碍(ED)。目前,国内尚未有同时治疗BPH-LUTS和ED的药物上市,复达那非弥补了该领域的空白。本品共2个规格片剂,其中原料和1个规格的制剂进入审评阶段的时间是2月2日,本周第2个规格进入在审评阶段。
7、恩替诺特片:本品由亿腾药业申报,英文名Entinostat,2015年3月进入审评中心,为特殊审批品种,目前已获批临床。恩替诺特是一种研究中的组蛋白去乙酰化酶(HDAC)抑制剂,用于晚期乳腺癌(III 期)和非小细胞肺癌的治疗(II 期)。这个由美国Syndax制药研发的药物2013年获得FDA突破性疗法认定。
8、CVI-LM001及片:本品是西威埃医药申报的1.1类小分子PCSK9抑制剂,用于治疗高血脂。CVI-LM001在2014年就已经进入审评中心,尽管是重大专项和特殊审批品种,但是中间经过一次发补,目前处于在审批阶段,获批临床。
9、Taselisib片:本品由罗氏开发,是一种PIK3CA的选择性抑制剂,用于治疗乳腺癌、原发性子宫收缩浆液性癌等。本品最早在国内2015年3月承办,为特殊审批品种,目前已获批临床。此外,本品2015年12月又提交临床申请。
10、AZD3759及片:本品由阿斯利康开发,是一种用于治疗中枢神经系统转移的非小细胞肺癌的新药,针对EGFR突变。本品2015年4月23日进入审评中心,为特殊审批品种,目前已获批临床。
11、HS-10241及片:本品由江苏豪森开发,是一种c-Met抑制剂,用于治疗肿瘤。HS-10241于2015年4月进入审评中心,为特殊审批品种,目前已获批临床。

分享到:







 相关新闻
相关新闻